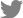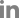|
 |
| Ann Optom Contact Lens > Volume 20(4); 2021 > Article |
|
Abstract
ļ¬®ņĀü
ļ╣äņĀäĒśĢņĀüņØĖ ņ”ØņäĖļź╝ ļ│┤ņØ┤ļŖö ņ¢æņĢł ņŗ£ņŗĀĻ▓ĮņŚ╝ ĒÖśņ×ÉņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØä ņ¦äļŗ©ĒĢśĻ│Ā ņ╣śļŻīĒĢ£ ņ”ØļĪĆļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”ØļĪĆņÜöņĢĮ
34ņäĖ ņŚ¼ņ×É ĒÖśņ×ÉĻ░Ć 3ņŻ╝ ņĀä ĻĖēņä▒ ņ▓ÖņłśņŚ╝ ņ”ØņäĖņÖĆ 2ņŻ╝ ņĀä ņ¢æņĢł ņŗ£ļĀźņĀĆĒĢś ņåīĻ▓¼ņ£╝ļĪ£ ņŗĀĻ▓ĮĻ│╝ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ņØśņ”ØĒĢś Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ ņĀĢļ¦ź ņÜöļ▓ĢņØä ļ░øņĢśņ£╝ļéś ņŗ£ļĀźĒśĖņĀäņØ┤ ņŚåņ¢┤ ņĢłĻ│╝ņŚÉ ņØśļó░ļÉśņŚłļŗż. ņ┤łņ¦ä ņŗ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź ņ¢æņĢł ļ¬©ļæÉ 0.04, ņóīņĢłņØś ļīĆĻĄ¼ņŗ¼ļÅÖĻ│ĄņÜ┤ļÅÖņןņĢĀņÖĆ Ishihara ņāēĻ░üĻ▓Ćņé¼ņŚÉņä£ ņ¢æņĢł 1/17, ņĢłņĀĆĻ▓Ćņé¼ņāü ņŗ£ņŗĀĻ▓Įņ£ĀļæÉļČĆņóģņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ļćī ļ░Å ņ▓Öņłś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņØś T2 Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ņĀäļæÉņŚĮ Ēö╝ņ¦łĒĢś ļ░▒ņ¦ł, ņ¢æņĢł ņŗ£ņŗĀĻ▓Į ĻĄÉņ░© ļČĆņ£ä ļ░Å ņóīņĖĪ ĻĄ¼Ēøä ņŗ£ņŗĀĻ▓Į ļČäņĀł, ņŚ░ņłśņÖĆ C2ņŚÉņä£ C5 ļČäņĀłņŚÉ ĻĖĖĻ▓ī Ļ▒Ėņ╣£ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. Ēśłņ▓ŁĻ▓Ćņé¼ņŚÉņä£ ĒĢŁņĢäņ┐ĀņĢäĒżļ”░-4 ĒĢŁņ▓┤(aquaproin-4 immunogloblin G antibody [AQP4-IgG Ab])ļŖö ņØīņä▒ņØ┤ņŚłļŗż. Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ ļ│ĄņÜ® Ēøä 1ļŗ¼ņ¦Ė ņ¢æņĢł ņŗ£ļĀź 1.0/0.8ļĪ£ Ē¢źņāüļÉśņŚłĻ│Ā, ņØ┤Ēøä 4ļģä ļÅÖņĢł ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆļź╝ ņ£Āņ¦ĆĒĢśļ®░ ņ×¼ļ░£ ņŚåņØ┤ ņ¦Ćļé┤ļŹś ņżæ ņČöņĀü ņåīņŗżļÉśņŚłļŗż.
Abstract
Purpose
We report a case of multiple sclerosis with bilateral optic neuritis that was atypical in terms of both the clinical signs and symptoms.
Case summary
A 34-year-old female visited the department of neurology with a complaint of sudden-onset, left lower extremity weakness and numbness that had developed 3 weeks prior, and bilateral blurred vision that had commenced 2 weeks prior. The patient was diagnosed with multiple sclerosis and prescribed high-dose intravenous methylprednisolone for 3 days, but the blurred vision did not improve. The patient was referred to the ophthalmology department. The initial best-corrected visual acuity was 0.04 in both eyes, and the relative afferent pupillary defect test was positive for the left eye. The Ishihara color test scores were 1/17 for both eyes. No optic disc swelling was evident on fundus examination. Brain and spine magnetic resonance imaging (T2-weighted) performed during the initial visit revealed lesions of high signal intensity in the frontal, subcortical white matter; the optic chiasm; the left retrobulbar optic segment; the medulla; and the spinal C2-5 processes. Aquaproin-4 immunogloblin G antibody (AQP4-IgG Ab) was not detected in serum. One month after prescription of the oral steroid, the vision improved to 1.0 in the right and 0.8 in the left eye. The patient was lost to follow-up after prescription of interferon-beta for 4 years, without recurrence.
ņĀŖņØĆ ņä▒ņØĖņŚÉņä£ ņżæņČöņŗĀĻ▓ĮĻ│ä Ēāłņłśņ┤łņ¦łĒÖś ņżæ Ļ░Ćņן ĒØöĒĢ£ ĒśĢĒā£ņØĖ ļŗżļ░£Ļ▓ĮĒÖöņ”Ø(multiple sclerosis, MS)ņØĆ ļćī, ņ▓Öņłś, ļśÉļŖö ņŗ£ņŗĀĻ▓ĮņŚÉ ļ¦īņä▒ņĀüņ£╝ļĪ£ ļ░śļ│ĄļÉśļŖö ņ×ÉĻ░Ćļ®┤ņŚŁņä▒ Ēāłņłśņ┤łņ¦łĒÖśņ£╝ļĪ£, ļ│æļ│ĆņØ┤ ņŗ£Ļ░äĻ│╝ Ļ│ĄĻ░äņĀü ņĖĪļ®┤ņŚÉņä£ ņŚ¼ļ¤¼ ļ▓ł(dissemination in time, DIT), ņŚ¼ļ¤¼ ļČĆņ£ä(dissemination in space, DIS)ņŚÉņä£ ļ░£ņāØļÉ©ņØä ĒŖ╣ņ¦Ģņ£╝ļĪ£ ņ¦Ćļŗīļŗż. ņ╣©ļ▓öļÉśļŖö ņ£äņ╣śņŚÉ ļö░ļØ╝ ļŗżņ¢æĒĢ£ ņ×äņāüņ¢æņāüņØä ļ│┤ņØ╝ ņłś ņ׳ļŖöļŹ░, ĻĘĖņżæ ņŗ£ņŗĀĻ▓ĮņŚ╝ņØĆ ņĢĮ 20%ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØś ņ┤łĻĖ░ ņ”ØĒøäļĪ£, 50%ņŚÉņä£ ļ│æņØś Ļ▓ĮĻ│╝ ņżæņŚÉ ļ░£ņāØļÉĀ ņłś ņ׳ņ¢┤ ņĢłĻ│╝ ņØśņé¼ļĪ£ņä£ ņŻ╝ņØśļź╝ ņÜöĒĢ£ļŗż[1].
ņØ╝ļ░śņĀüņ£╝ļĪ£ ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ņŚ░Ļ┤Ć ņŗ£ņŗĀĻ▓ĮņŚ╝(MS-optic neuritis [ON])ņØś Ļ▓ĮņÜ░ ĻĄ¼Ēøäņŗ£ņŗĀĻ▓ĮņŚ╝ņØ┤ ĒØöĒĢśļ®░, ļŗ©ņĢłņØś ĻĖēņä▒ ņŗ£ļĀźņĀĆĒĢś, ņĢłĻĄ¼ņÜ┤ļÅÖ ņŗ£ ĒåĄņ”Ø, ņāēĻ░ü ļ░Å ņŗ£ņĢ╝ ņØ┤ņāü ļō▒ņØś ņ”ØņäĖļź╝ ļ│┤ņØĖļŗż[1]. ĒĢśņ¦Ćļ¦ī ļ╣äņĀäĒśĢņĀü ņŗ£ņŗĀĻ▓ĮņŚ╝ ņ”ØņäĖļź╝ ļ│┤ņØ┤ļŖö Ļ▓ĮņÜ░ņŚÉļŖö ļÅÖņ¢æņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Øļ│┤ļŗż ļ░£ņāØ ļ╣łļÅäĻ░Ć ļŹö ļåÆņØĆ ņŗ£ņŗĀĻ▓Įņ▓ÖņłśņŚ╝ ļ▓öņŻ╝ņ¦łĒÖś(neuromyelitis optica spectrum disorder, NMOSD), myelin oligodendrocyte glycoprotein immunogloblin G (MOG-IgG) ņ¢æņä▒ ņŗ£ņŗĀĻ▓ĮņŚ╝ ļō▒ ļŗżļźĖ ņżæņČöņŗĀĻ▓ĮĻ│ä Ēāłņłśņ┤łņ¦łĒÖśĻ│╝ņØś Ļ░Éļ│äņØ┤ ņżæņÜöĒĢ£ļŹ░, Ļ░üĻ░ü ņ¦łļ│æĒŖ╣ņØ┤ĒĢŁņ▓┤ļź╝ ņ¦ĆļŗłļŖö ĒŖ╣ņ¦ĢņØ┤ ņ׳ņ£╝ļéś ņØīņä▒ņØĖ Ļ▓ĮņÜ░Ļ░Ć ņ׳ņ¢┤ Ļ░Éļ│äņ¦äļŗ©ņØ┤ ņ¢┤ļĀżņÜĖ ņłś ņ׳ļŗż[1-3]. ĒŖ╣Ē׳, ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆ(interferon-beta)ļéś ĻĖĆļØ╝Ēŗ░ļØ╝ļ©ĖņĢäņäĖĒģīņØ┤ĒŖĖ(glatiramer acetate)ļź╝ ņĪ░ĻĖ░ņŚÉ ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ĒÖśņ×ÉņŚÉ ņĀüņÜ®ĒĢĀ Ļ▓ĮņÜ░ ņ×äņāüļŗ©ļÅģņ”ØĒøäĻĄ░(clinically isolated syndrome)ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Øņ£╝ļĪ£ņØś ņĀäĒÖśņØ┤ļéś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüĻ▓Ćņé¼ņāü ņāłļĪ£ņÜ┤ T2 ļ│æļ│ĆņØś ļ░£ņāØņØä ņżäņØ╝ ņłś ņ׳ņ£╝ļéś, ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆ, ļéśĒāłļ”¼ņŻ╝ļ¦Ö(natalizumab), ĒĢæĻ│©ļ”¼ļ¬©ļō£(fingolimod)ņÖĆ Ļ░ÖņØĆ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØś ņ╣śļŻīļź╝ neuromyelitis optica (NMO)-IgG ņ¢æņä▒ ņŗ£ņŗĀĻ▓ĮņŚ╝ņŚÉ ņĀüņÜ®ĒĢĀ Ļ▓ĮņÜ░ ņ¦łĒÖśņØś Ļ▓ĮĻ│╝ļź╝ ņĢģĒÖöņŗ£Ēé¼ ņłś ņ׳ļŗż[1-3]. ļ│Ė ņ”ØļĪĆņŚÉņä£ ņĀĆņ×ÉļōżņØĆ ņĀŖņØĆ ņä▒ņØĖ ĒÖśņ×ÉņŚÉņä£ ļ╣äņĀäĒśĢņĀüņØĖ ņ¢æņĢł ņŗ£ņŗĀĻ▓ĮņŚ╝ņØä ļ│┤ņØ┤ļŖö ļō£ļ¼Ė ĒśĢĒā£ņØś ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØä NMOSDĻ│╝ Ļ░Éļ│äĒĢśĻ│Ā ņĀüņĀłĒ׳ ņ╣śļŻīĒĢ£ ņ”ØļĪĆļź╝ Ļ▓ĮĒŚśĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
ļ│Ė ņ”ØļĪĆ ļ│┤Ļ│ĀļŖö Ļ░ĆĒå©ļ”ŁļīĆĒĢÖĻĄÉ ņŚ¼ņØśļÅäņä▒ļ¬©ļ│æņøÉņØś ņ×äņāüņŚ░ĻĄ¼ņ£żļ”¼ņ£äņøÉĒÜī(IRB)ņŚÉ ņØśĒĢ┤ ļ®┤ņĀ£ļÉśņŚłļŗż(ņŖ╣ņØĖ ļ▓łĒśĖ: SC21ZESE0039).
ĒŖ╣ņØ┤ ĻĖ░ņĀĆ ņ¦łĒÖśņØ┤ ņŚåļŖö 34ņäĖ ņŚ¼ņ×É ĒÖśņ×ÉĻ░Ć 3ņŻ╝ ņĀä Ļ░æņ×ÉĻĖ░ ņŗ£ņ×æļÉ£ ņóīņĖĪ ĒĢśņ¦Ć Ļ░ÉĻ░üņĀĆĒĢśņÖĆ ļ│┤Ē¢ē ņןņĢĀ, 2ņŻ╝ ņĀäļČĆĒä░ ļ░░ļć© ņןņĢĀņÖĆ ĒĢ©Ļ╗ś 1ņŻ╝ Ļ░äĻ▓®ņ£╝ļĪ£ ņóīņĢłņŚÉņä£ ņÜ░ņĢłņ£╝ļĪ£ ņ¦äĒ¢ēļÉśļŖö ņ¢æņĢł ņŗ£ļĀźņĀĆĒĢśļź╝ ĒśĖņåīĒĢśņśĆļŗż. ņØ┤ņŚÉ ņŗĀĻ▓ĮĻ│╝ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ņØśņ”ØĒĢś Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ Methylprednisolone (Predisol┬« 250 mg, 4 times/day, 3 days) ņĀĢļ¦ź ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ņØ┤ņ¢┤ Ļ▓ĮĻĄ¼ ņŖżĒģīļĪ£ņØ┤ļō£ ņ£Āņ¦Ć ņżæņŚÉ ņ¢æņĢł ņŗ£ļĀźņĀĆĒĢśĻ░Ć ĒśĖņĀäļÉśņ¦Ć ņĢŖņĢä ņ╣śļŻī Ēøä 4ņØ╝ņ¦Ė ņĢłĻ│╝ņŚÉ ņØśļó░ļÉśņŚłļŗż.
ņĢłĻ│╝ ņ┤łņ¦ä ļŗ╣ņŗ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ņ¢æņĢł ļ¬©ļæÉ 0.04ņśĆĻ│Ā, ņóīņĢłņØś ņāüļīĆĻĄ¼ņŗ¼ļÅÖĻ│ĄņÜ┤ļÅÖņןņĢĀ(relative afferent pupillary defect, RAPD)ņÖĆ Isihara ņāēĻ░üĻ▓Ćņé¼ņŚÉņä£ ņ¢æņĢł 1/17Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. ņĢłņĀĆĻ▓Ćņé¼ņāü ņŗ£ņŗĀĻ▓Įņ£ĀļæÉļČĆņóģņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśņ£╝ļ®░(Fig. 1A), ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄņ┤¼ņśüņāü ņ¢æņĢł ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄ(retinal nerve fiber layer) ļ░Å ņŗĀĻ▓ĮņĀłņäĖĒżņĖĄ(ganglion cell layer, GCL) ļæÉĻ╗śļŖö ņĀĢņāü ļ▓öņ£äņśĆļŗż(Fig. 1B, C). ļ¼Ėņ¢æ ņŗ£ņ£Āļ░£ņĀäņ£äĻ▓Ćņé¼ļĪ£ļŖö ņ¢æņĢł(ĒŖ╣Ē׳ ņÜ░ņĢł) P100 ņ×Āļ│ĄĻĖ░ ņ¦ĆņŚ░ņØä ļ│┤ņśĆĻ│Ā, ĒŚśĒöäļ”¼ ņŗ£ņĢ╝ Ļ▓Ćņé¼ņŚÉņä£ļŖö ņ¢æņĢł ņØ┤ņĖĪ ļ░śļ¦╣ ņåīĻ▓¼ņØ┤ ļ│┤ņśĆļŗż(Fig. 1D).
ņŗĀĻ▓ĮĻ│╝ ņ×ģņøÉ ņŗ£ ņŗ£Ē¢ēĒĢ£ ļćīņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüĻ▓Ćņé¼ņØś T2 Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ļćīļ¤ē, ņ¢æņĖĪ ņĀäļæÉņŚĮ Ēö╝ņ¦łĒĢśļ░▒ņ¦ł, ņÜ░ņĖĪņØś ņŚ░ņłś ļ░Å ĻĄÉļćī, ņåīļćīĻ░üņŚÉ ļŗżļ░£ņä▒ņØś Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśņŚłņ£╝ļ®░, ņ¢æņĢł ņŗ£ņŗĀĻ▓Į ĻĄÉņ░© ļČĆņ£ä ļ░Å ņóīņĖĪ ĻĄ¼Ēøä ņŗ£ņŗĀĻ▓Į ļČäņĀłņŚÉ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖĻ░Ć ļ│┤ņśĆļŗż(Fig. 2A). ņ▓Öņłś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüĻ▓Ćņé¼ņØś T2-fluid attenuated inversion recovery (FLAIR) Ļ░ĢņĪ░ņśüņāüņŚÉņä£ļŖö ņŚ░ņłśņÖĆ C2ņŚÉņä£ C5 ļČäņĀłņŚÉ ĻĖĖĻ▓ī Ļ▒Ėņ╣£ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 2B). Ēśłņ▓ŁĻ▓Ćņé¼ņŚÉņä£ ĒĢŁņĢäņ┐ĀņĢäĒżļ”░-4 ĒĢŁņ▓┤(AQP-4 IgG Ab) ļ░Å ņ×ÉĻ░ĆĒĢŁņ▓┤ ņØīņä▒, ļćīņ▓ÖņłśņĢĪĻ▓Ćņé¼ņŚÉņä£ ņś¼ļ”¼Ļ│ĀĒü┤ļĪĀļØĀ(oligoclonal band) ņØīņä▒, ņäĖĒżņ”ØĻ░Ćņ”Ø(pleocytosis)ņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśņ£╝ļéś, ņĢīļČĆļ»╝ņäĖĒżĒĢ┤ļ”¼(albumincocytologic dissociation)ļź╝ ļ│┤ņśĆļŗż.
ņŗĀĻ▓ĮĻ│╝ņŚÉņä£ Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ ņĀĢļ¦ź ņ╣śļŻī Ēøä Ļ▓ĮĻĄ¼ņÜ® Prednisolone (Solondo Tab┬«, Yuhan Corp., Chungju, Korea) 60 mgņØä ņŗ£ņ×æņ£╝ļĪ£ 1ņŻ╝ņØ╝ ļŗ©ņ£äļĪ£ 50 mg, 40 mg, 30 mg, 20 mg, 10 mgņ£╝ļĪ£ Ļ░Éļ¤ēĒĢśņŚ¼ ļ│ĄņÜ®ĒĢśņśĆļŗż. ņŖżĒģīļĪ£ņØ┤ļō£ ņ╣śļŻī 1ļŗ¼ Ēøä ĻĖēņä▒ ņ▓ÖņłśņŚ╝ ņ”ØņäĖļŖö ĒśĖņĀäļÉśņŚłĻ│Ā, ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź ņÜ░ņĢł 1.0, ņóīņĢł 0.8ņØ┤ņŚłņ£╝ļ®░, ņóīņĢł RAPD ņ¢æņä▒, ņāēĻ░üĻ▓Ćņé¼ļŖö ņÜ░ņĢł 12/17, ņóīņĢł 6/17ņØ┤ņŚłļŗż. ņĢłņĀĆĻ▓Ćņé¼ņāü ņŗ£ņŗĀĻ▓Įņ£ĀļæÉļČĆņóģņØ┤ļéś ņ░Įļ░▒ņØĆ ņŚåņŚłļŗż(Fig. 3A). ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄņ┤¼ņśüņāü GCL ļæÉĻ╗śļŖö Ļ░ÉņåīļÉśņŚłņ£╝ļ®░(Fig. 3B), ĒŚśĒöäļ”¼ņŗ£ņĢ╝Ļ▓Ćņé¼ņŚÉņä£ ņ¢æņĢł ņØ┤ņĖĪ ļ░śļ¦╣ ņåīĻ▓¼ņØĆ ļŗżņåī ĒśĖņĀäļÉśņŚłļŗż(Fig. 3C). ļ░£ļ│æ 5Ļ░£ņøö ĒøäļČĆĒä░ ņĢĮ 4ļģä ļÅÖņĢł ņŗĀĻ▓ĮĻ│╝ņŚÉņä£ ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆ(Rebif┬«, Merck Serono, Geneva, Switzerland)ļź╝ ņ£Āņ¦ĆĒĢśņśĆĻ│Ā, ļ░£ļ│æ 1ļģäņ¦Ė ņŗ£Ē¢ēĒĢ£ ņČöņĀü ļćīņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüĻ▓Ćņé¼ņāü ņØ┤ņĀäņØś T2-FLAIR Ļ░ĢņĪ░ ņśüņāüņŚÉņä£ Ļ┤Ćņ░░ļÉ£ ļŗżļ░£ņä▒ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖļŖö ĒśĖņĀäļÉśņŚłļŗż(Fig. 4). ļ░£ļ│æ Ēøä 4ļģäņ¦Ė Ļ░äĒŚÉņĀü ņ£ĀĒåĀĒöä Ēśäņāü(uhthoffŌĆÖs phenomenon)ņØä ļ│┤ņśĆņ£╝ļéś ņŗ£ļĀźņĀĆĒĢś ļō▒ņØś ņ×¼ļ░£ ņåīĻ▓¼ ņŚåņØ┤ ņ¦Ćļé┤ļŹś ņżæ ņČöņĀü ņåīņŗżļÉśņŚłļŗż.
ņŗ£ņŗĀĻ▓ĮņŚ╝ņØ┤ļ×Ć ņŗ£ņŗĀĻ▓ĮņŚÉ ļ░£ņāØļÉśļŖö ņŚ╝ņ”Øņä▒ Ēāłņłśņ┤łņ¦łĒÖśņ£╝ļĪ£, ņĀäĒśĢņĀüņ£╝ļĪ£ ļŗ©ņĢłņØś ĻĖēņä▒ ņŗ£ļĀźņĀĆĒĢś, ņĢłĻĄ¼ņÜ┤ļÅÖ ņŗ£ ņĢłĻĄ¼ņŻ╝ņ£ä ĒåĄņ”Ø, ņŗ£ņĢ╝ ļ░Å ņāēĻ░üņĀĆĒĢś ļō▒ņØś ņ”ØņäĖļź╝ ļ│┤ņØĖļŗż[1,4]. ņØ┤ņØś ļīĆĒæ£ņĀü ņøÉņØĖņ£╝ļĪ£ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØ┤ ņ׳ņ£╝ļéś, ņŗ£ņŗĀĻ▓ĮņŚ╝ņØ┤ ļ╣äņĀäĒśĢņĀüņØĖ ņ”ØņäĖ-ņ”ē, ņĢłĒåĄņØ┤ ļÅÖļ░śļÉśņ¦Ć ņĢŖĻ▒░ļéś, ļ░£ļ│æ ņ┤łĻĖ░ļČĆĒä░ ņŗ£ņŗĀĻ▓Įņ£ĀļæÉ ņ░Įļ░▒ņØä ļ│┤ņØ┤ļŖö Ļ▓ĮņÜ░, ļ│æņØś Ļ▓ĮĻ│╝ ņ¦äĒ¢ē ņżæ ņŗ£ļĀźĒśĖņĀäņØ┤ ņŚåĻ│Ā, ņ¢æņĢł ļ░£ņāØ ļō▒ņØä ļ│┤ņØ┤ļŖö Ļ▓ĮņÜ░ņŚÉļŖö NMO-IgG ņŚ░Ļ┤Ć NMOSD, MOG-IgG ņ¢æņä▒ ņŗ£ņŗĀĻ▓ĮņŚ╝, ĻĖēņä▒ Ēīīņóģņä▒ ļćīņ▓ÖņłśņŚ╝(acute disseminated encephalomyelitis)Ļ│╝ Ļ░ÖņØĆ ļŗżļźĖ ņżæņČöņŗĀĻ▓ĮĻ│ä Ēāłņłśņ┤łņ¦łĒÖś, ņ×ÉĻ░Ćļ®┤ņŚŁņ¦łĒÖś ļō▒ ņŚ¼ļ¤¼ ņøÉņØĖĻ│╝ņØś Ļ░Éļ│äņØ┤ ļ░śļō£ņŗ£ ĒĢäņÜöĒĢśļŗż[1,2,5].
MS-ONņØĆ ļ¦Éņ┤ł ĒśłņĢĪņØś T ļ”╝ĒöäĻĄ¼Ļ░Ć ĒśłņĢĪļćīņןļ▓ĮņØä ĒåĄĻ│╝ĒĢ┤ ņżæņČöņŗĀĻ▓ĮĻ│äņŚÉ ļ¦īņä▒ ņŗĀĻ▓Į ņåÉņāüņØä ņØ╝ņ£╝ĒéżĻ▓ī ļÉśļ®░ ļ░£ņāØļÉśļŖöļŹ░, 2017ļģä Ļ░£ņĀĢļÉ£ McDonald CriteriaņŚÉ ņØśĒĢśļ®┤ ņ”ØņāüĻ│╝ ļ│æļ│ĆņØ┤ DISņÖĆ DITņØ┤ ņ׳ņ£╝ļ®░ ļŗżļźĖ ņ£Āņé¼ ņ¦łĒÖśņØ┤ ļ░░ņĀ£ļÉ£ Ļ▓ĮņÜ░(exclusion of diagnosis)ļź╝ ļ¦ÉĒĢ£ļŗż[3,5]. ļ░śļ®┤, NMO-IgG ņŚ░Ļ┤Ć ņŗ£ņŗĀĻ▓ĮņŚ╝(ņØ┤ĒĢś, NMO-ON)ņØĆ AQP4-IgG, ņ”ē, ĒśłņĢĪļćīņןļ▓ĮņØś ĻĄ¼ņä▒ ļ¼╝ņ¦łņØĖ ļ│äņĢäĻĄÉņäĖĒż(astrocyte)ņŚÉ ņĪ┤ņ×¼ĒĢśļŖö AQP-4 ļŗ©ļ░▒ņ¦łņŚÉ ļīĆĒĢ£ ņ×ÉĻ░Ćļ®┤ņŚŁĒĢŁņ▓┤ļĪ£ ņØĖĒĢśņŚ¼, MOG-IgG ņŚ░Ļ┤Ć ņŗ£ņŗĀĻ▓ĮņŚ╝(ņØ┤ĒĢś, MOG-ON)ņØĆ ņżæņČöņŗĀĻ▓ĮĻ│ä ņŗĀĻ▓Įņłśņ┤ł(myelin)ņØś ĻĄ¼ņä▒ļ¼╝ņ¦łņØĖ ĒؼņåīļÅīĻĖ░ņĢäĻĄÉņäĖĒż(oligodendrocyte)ņØś Ēæ£ļ®┤ ļŗ©ļ░▒ņ¦łņŚÉ ļīĆĒĢ£ ĒĢŁņ▓┤(anti-MOG Ab)ļĪ£ ņØĖĒĢśņŚ¼ ņżæņČöņŗĀĻ▓ĮĻ│äĻ░Ć ņåÉņāüņØä ļ░øņ£╝ļ®░ ņ£Āļ░£ļÉ£ļŗż[4,6]. ļæÉ ĒĢŁņ▓┤ ļ¬©ļæÉ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņŚÉņä£ ļ░£ĒśäļÉśņ¦Ć ņĢŖņ£╝ļ®░, Ļ░üĻ░ü ņ¦łļ│æ ĒŖ╣ņØ┤ņĀüņØĖ ņ×äņāüĻ▓ĮĻ│╝ļź╝ ļ│┤ņØ┤Ļ▓ī ļÉśļéś, AQP-4 AbļŖö NMO-ONņØś 70% Ļ░Ćļ¤ēņŚÉņä£ļ¦ī ļ░£ĒśäļÉśļ®░, anti-MOG-AbļŖö AQP-4 Ab ņØīņä▒ ĒÖśņ×ÉĻĄ░ņØś 25%ņŚÉņä£ ļ░£ĒśäĒĢśĻ▓ī ļÉśņ¢┤ ņĀĢĒÖĢĒĢ£ ņ×äņāüņ¢æņāüņØś ĒīīņĢģĻ│╝ ņĀüņĀłĒĢ£ ņ¦äļŗ©ļ▓ĢņØś ņĀüņÜ®ņØ┤ ņżæņÜöĒĢśļŗż[2,4,6,7].
ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļŖö ņØ╝ļ░śņĀüņØĖ MS-ONņØś Ļ▓ĮĻ│╝ņÖĆļŖö ļŗ¼ļØ╝ NMOSDņÖĆņØś Ļ░Éļ│äņØ┤ ņ¢┤ļĀżņøĀļŗż. ņĀäĒśĢņĀüņØĖ MS-ONņØś Ļ▓ĮņÜ░ ņŗ£ļĀźņĀĆĒĢśĻ░Ć ļŗ©ņĢłņŚÉ ĻĖēņä▒ ļśÉļŖö ņĢäĻĖēņä▒ņ£╝ļĪ£ ļ░£ņāØĒĢśņŚ¼ ņłśņØ╝ņŚÉņä£ 2ņŻ╝Ļ░Ćļ¤ē ņ¦äĒ¢ēĒĢśļŗż ņ╣śļŻī ņŚ¼ļČĆņÖĆ ļ¼┤Ļ┤ĆĒĢśĻ▓ī 90% ņØ┤ņāüņŚÉņä£ 2-3ņŻ╝ ņØ┤ļé┤ļĪ£ ņ×ÉņŚ░ ĒśĖņĀäļÉ£ļŗż[1,5]. ņ┤łĻĖ░ ņŗ£ļĀźņåīņŗżņØĆ Ļ▓ĮĒĢ£ Ļ▓ĮņÜ░(visual acuity 20/20)ļČĆĒä░ ņŗ¼ĒĢ£ Ļ▓ĮņÜ░(Ļ┤æĻ░üļ¼┤)Ļ╣īņ¦Ć ļŗżņ¢æĒĢĀ ņłś ņ׳ļŗż[1,5]. ĒĢśņ¦Ćļ¦ī ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļŖö ļ╣äņĀäĒśĢņĀüņØĖ ņ¢æņĢł ņŗ£ņŗĀĻ▓ĮņŚ╝ņØś ņ¢æņāüņØä ļ│┤ņśĆļŗż. ļ░£ļ│æ ņ┤łĻĖ░ļČĆĒä░ ņŗ¼ĒĢ£ ņŗ£ļĀźņĀĆĒĢśļź╝ ļ│┤ņØ┤ļ®░ ļŗ©ņĢł ļ░£ļ│æ 1ņŻ╝ Ēøä ļ╣Āļź┤Ļ▓ī ņ¢æņĢłņ£╝ļĪ£ ņ¦äĒ¢ēļÉśļŖö ņŗ£ņŗĀĻ▓ĮņŚ╝ņØś ĒśĢĒā£ņśĆļŗż. ņØ┤ļŖö MS-ONļ│┤ļŗżļŖö ņ┤łĻĖ░ ņŗ£ļĀźņåīņŗżņØ┤ ļŹö ņŗ¼ĒĢśļ®░ ņ¢æņĢłņä▒ņØś Ļ▓ĮĒ¢źņØ┤ Ļ░ĢĒĢ£ NMO-ONņØś Ļ▓ĮĻ│╝ņÖĆ ļŹö Ļ░ĆĻ╣Øļŗż[6].
ļśÉĒĢ£ ļ│Ė ņ”ØļĪĆņŚÉņä£ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü ņåīĻ▓¼ļÅä MS-ONļ│┤ļŗżļŖö NMO-ONņØä ļŹö ņŗ£ņé¼ĒĢ£ļŗż. ļćīņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņāü ĒÖśņ×ÉļŖö ņŗ£ņŗĀĻ▓Į ĻĄÉņ░© ļČĆņ£äļź╝ ņ╣©ļ▓öĒĢśļ®░ ņŗ£ņĢ╝Ļ▓Ćņé¼ņŚÉņä£ ņØ┤ņÖĆ ņØ╝ņ╣śĒĢśļŖö ņ¢æņĢł ņØ┤ņĖĪ ļ░śļ¦╣ ņåīĻ▓¼ņØä ļ│┤ņśĆļŖöļŹ░, ņØ┤ļŖö NMO-ONņŚÉ ļŹö ņĀüĒĢ®ĒĢ£ ņ×äņāü ņåīĻ▓¼ņ£╝ļĪ£, NMO-ONņØś Ļ▓ĮņÜ░ ņŗ£ņŗĀĻ▓ĮņŚ╝ņØ┤ ņ¢æņĖĪ ņĢłĻĄ¼ ļÆż, ņŗ£ņŗĀĻ▓Į ĻĄÉņ░©Ļ╣īņ¦Ć ĻĖĖĻ▓ī ņ╣©ļ▓öļÉśņ¢┤ MS-ONļ│┤ļŗż ļ░£ņāØ ņ┤łĻĖ░ ņ¢æņĢłņŚÉ ļŹö ņŗ¼ĒĢ£ ņŗ£ļĀźņĀĆĒĢśļź╝ ļ│┤ņØ┤ļŖö Ļ▓ĮĒ¢źņØ┤ ņ׳ļŗż[2,3]. ļŹöļČłņ¢┤, ļćīņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņāü Ēö╝ņ¦łĒĢś ļ░▒ņ¦łņŚÉ ļŗżļ░£ņä▒ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖļź╝ ļ│┤ņØ┤ļŖö ņĀÉņØĆ ļŗżļ░£Ļ▓ĮĒÖöņ”ØĻ│╝ ņØ╝ņ╣śĒĢśļéś, ļćīļ¤ē, ņÜ░ņĖĪņØś ņŚ░ņłś ļ░Å ĻĄÉļćī, ņåīļćīĻ░ü ļō▒ ļćīņŗżņ¦łņŚÉ Ļ┤æļ▓öņ£äĒĢ£ ļ│æļ│ĆņØä ļ│┤ņØ┤ļŖö ņĀÉĻ│╝ ņ▓Öņłś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņāü ņŚ░ņłśņÖĆ ņāüļČĆ Ļ▓ĮņČö ņ▓Öņłś ļČäņĀł 3Ļ░£ ņØ┤ņāüņŚÉ Ļ▒Ėņ╣£ ĻĖ┤ ņ▓ÖņłśņŚ╝ ņåīĻ▓¼ņØĆ NMOSDņØś ņ¦äļŗ©ņŚÉ ļŹö Ļ░ĆĻ╣Øļŗż[8]. ļö░ļØ╝ņä£ ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļŖö AQP-4 AbļŖö ņØīņä▒ņØ┤ņŚłņØīņŚÉļÅä ņ×äņāüņĀü ņåīĻ▓¼Ļ│╝ ņśüņāüĻ▓Ćņé¼ņŚÉņä£ ņĀäĒśĢņĀüņØĖ ļŗżļ░£Ļ▓ĮĒÖöņ”ØĻ│╝ ļ¦×ņ¦Ć ņĢŖņĢä ŌĆśĒśłņ▓ŁĒĢÖņĀü ņØīņä▒ŌĆÖ ņŗ£ņŗĀĻ▓Įņ▓ÖņłśņŚ╝ļ▓öņŻ╝ņ¦łĒÖś(seronegative NMOSD) Ļ░ĆļŖźņä▒ņØä ļ░░ņĀ£ĒĢĀ ņłś ņŚåņŚłļŗż.
ĻĘĖļ¤╝ņŚÉļÅä ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņØ┤ņ£ĀļĪ£ ŌĆśĒśłņ▓ŁĒĢÖņĀü ņØīņä▒ŌĆÖ ņŗ£ņŗĀĻ▓Įņ▓ÖņłśņŚ╝ļ▓öņŻ╝ņ¦łĒÖśļ│┤ļŗż ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ņ¦äļŗ© Ļ░ĆļŖźņä▒ņØ┤ ļŹö ļåÆņĢśļŗż. ļ©╝ņĀĆ, AQP-4 Ab ņØīņä▒ĻĄ░ņØś 25%ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Øņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ ļ│┤Ļ│ĀĻ░Ć ņ׳ņ£╝ļ®░[7], ļ│Ė ņ”ØļĪĆņŚÉņä£ ļćīņ▓ÖņłśņĢĪĻ▓Ćņé¼ņāü ņś¼ļ”¼Ļ│ĀĒü┤ļĪĀļØĀ ņØīņä▒ ņåīĻ▓¼ļ¦īņ£╝ļĪ£ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØä ļ░░ņĀ£ĒĢĀ ņłś ņŚåņŚłļŗż. ļćīņ▓ÖņłśņĢĪĻ▓Ćņé¼ņŚÉņä£ ņś¼ļ”¼Ļ│ĀĒü┤ļĪĀļØĀ(oligoclonal band) ņ¢æņä▒ ņåīĻ▓¼ņØĆ ņØ╝ļ░śņĀüņ£╝ļĪ£ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØä ļŹö ņŗ£ņé¼ĒĢśņ¦Ćļ¦ī, MS-ONņŚÉņä£ ņś¼ļ”¼Ļ│ĀĒü┤ļĪĀļØĀļŖö 69-97% Ļ░Ćļ¤ēņŚÉņä£ļ¦ī ņ¢æņä▒ņ£╝ļĪ£ Ļ┤Ćņ░░ļÉśņ¢┤ ļŗżļ░£Ļ▓ĮĒÖöņ”Øņ×äņŚÉļÅä ņś¼ļ”¼Ļ│ĀĒü┤ļĪĀļØĀĻ░Ć ņØīņä▒ņØ╝ ņłśļÅä ņ׳ļŗż[3]. ļæśņ¦ĖļĪ£, ņ¢æņĢł ņŗ£ņŗĀĻ▓ĮņŚ╝ ņåīĻ▓¼ņØ┤ ļ░śļō£ņŗ£ NMOSDļź╝ ņŗ£ņé¼ĒĢśņ¦ĆļŖö ņĢŖļŖöļŗż[3]. MS-ONņŚÉņä£ļÅä ļō£ļ¼╝Ļ▓ī ņ¢æņĢłņä▒ņ£╝ļĪ£ ļ░£ļ│æļÉ£ ņ”ØļĪĆĻ░Ć ļ│┤Ļ│ĀļÉśļŖöļŹ░, Srikajon et al [2]ņØś ņ”ØļĪĆ ļ│┤Ļ│ĀņŚÉņä£ 20ļ¬ģņØś ļŗżļ░£Ļ▓ĮĒÖöņ”Ø ĒÖśņ×É ņżæ 3ļ¬ģņØ┤ ņ┤łĻĖ░ ņŗ£ņŗĀĻ▓ĮņŚ╝ ļ░£ļ│æ ņŗ£ ņ¢æņĢłņØ┤ ļÅÖņŗ£ņŚÉ ņ╣©ļ▓öļÉśņŚłļŗżĻ│Ā ĒĢ£ļŗż. ņģŗņ¦Ė, NMO-ONņØś ņŗ£ļĀźņśłĒøäļŖö ļČłļ¤ēĒĢśļ®░ Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ņ╣śļŻīņŚÉ ņל ļ░śņØæĒĢśņ¦Ć ņĢŖņĢä ĒśłņןĻĄÉĒÖśņłĀĻ╣īņ¦Ć ĒĢäņÜöĒĢ£ ļŹ░ ļ░śĒĢ┤ ļ│Ė ņ”ØļĪĆņŚÉņä£ ņŗ£ļĀźņØĆ ņŖżĒģīļĪ£ņØ┤ļō£ņ╣śļŻī Ēøä ļ╣Āļź┤Ļ▓ī ĒÜīļ│ĄļÉśņŚłļŗż[6]. ļäĘņ¦Ė, Ļ┤æļ▓öņ£äĒĢ£ ĒÜĪļŗ©ņä▒ ņ▓ÖņłśņŚ╝(longitudinally extensive spinal cord lesion, LETM)ņØĆ NMOņØś ĒŖ╣ņ¦ĢņĀüņØĖ ņåīĻ▓¼ņØ┤ĻĖ░ļŖö ĒĢśļéś, LETM ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢ£ ņĮöĒśĖĒŖĖ ņŚ░ĻĄ¼ņŚÉņä£ ņĢĮ 6.5%ļ¦īņØ┤ ŌĆśtrue seronegativeŌĆÖ NMOļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż[7]. ļśÉĒĢ£, Ļ┤æļ▓öņ£äĒĢ£ ņŗ£ņŗĀĻ▓ĮņŚ╝(longitudinally extensive optic neuritis)ņØ┤ NMOņŚÉņä£ļ¦ī ĒŖ╣ņ¦ĢņĀüņØĖ ņåīĻ▓¼ņØĆ ņĢäļŗłļ®░, ļŗżļ░£Ļ▓ĮĒÖöņ”ØņØś 23% Ļ░Ćļ¤ēņŚÉņä£ļÅä Ļ┤Ćņ░░ļÉĀ ņłś ņ׳ĻĖ░ņŚÉ, ļ│Ė ņ”ØļĪĆņØś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü ņåīĻ▓¼ļ¦īņ£╝ļĪ£ NMOļĪ£ ĒÖĢņĀĢ ņ¦äļŗ©ņØä ļé┤ļ”┤ ņłśļŖö ņŚåņŚłļŗż[9]. ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£, ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļŖö 4ļģäĻ░ä ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆņØś ņ╣śļŻīņŚÉļÅä ņŗ£ņŗĀĻ▓ĮņŚ╝ņØ┤ ņ×¼ļ░£ĒĢśņ¦Ć ņĢŖņĢśļŗż. ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆ, ļéśĒāłļ”¼ņŻ╝ļ¦Ö, ĒĢæĻ│©ļ”¼ļ¬©ļō£ļŖö ļŗżļ░£Ļ▓ĮĒÖöņ”ØņŚÉņä£ ņ×¼ļ░£Ļ│╝ ņ¦łļ│æņØś ĒÖ£ņä▒ļÅäļź╝ ņżäņØ┤ĻĖ░ ņ£äĒĢ┤ ņĀüņÜ®ļÉśļŖö ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻīļ▓Ģņ£╝ļĪ£, ņØ┤ļōżņØ┤ NMOSDņŚÉ ņĀüņÜ®ļÉĀ Ļ▓ĮņÜ░ ņŗ¼Ļ░üĒĢ£ ļČĆņ×æņÜ®ņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŗż[2,10,11]. Palace et al [10]ņŚÉņä£ ļŗżļ░£Ļ▓ĮĒÖöņ”Øņ£╝ļĪ£ ņśżņ¦äļÉ£ NMOSD ĒÖśņ×ÉņŚÉņä£ ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆļź╝ ņĀüņÜ®ĒĢ£ Ļ▓ĮņÜ░ 3ļģä ļÆżļČĆĒä░ AQP-4 Ab titerĻ░Ć ņ”ØĻ░ĆĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņśĆņ£╝ļéś ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆļź╝ ņżæļŗ©ĒĢ£ ļÆż AQP-4 Ab ņłśņ╣śļŖö Ļ░ÉņåīĒĢśņśĆĻ│Ā, Warabi et al [11]ļŖö NMOSDņŚÉņä£ ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆĻ░Ć ņé¼ņÜ®ļÉĀ Ļ▓ĮņÜ░ ņŗ£ņŗĀĻ▓ĮĻ│╝ ņ▓ÖņłśņØś ņŚ╝ņ”Ø ņ×¼ļ░£ļźĀņØ┤ ļŹö ļåÆņĢśņ£╝ļ®░ ņŗ¼Ļ░üĒĢ£ ņŗ£ņŗĀĻ▓Į-ņ▓Öņłś Ēāłņłśņ┤ł ļ░śņØæņØä ņ£Āļ░£ĒĢ£ļŗżĻ│Ā ĒĢśņśĆļŗż.
ļ│Ė ņ”ØļĪĆņØś ņĀ£ĒĢ£ņĀÉņ£╝ļĪ£ ĒÖśņ×ÉĻ░Ć ņŗ£ļĀźņĀĆĒĢś ļ░£ļ│æ 3ņŻ╝ ĒøäņŚÉ ņ¦ĆņŚ░ ļé┤ņøÉĒĢśņŚ¼ ņĀĢĒÖĢĒĢ£ ļ░£ļ│æ ņ┤łĻĖ░ ņŗ£ļĀź ļō▒ ņĢłĻ│╝ Ļ▓Ćņé¼Ļ░Ć ņØ┤ļżäņ¦Ćņ¦Ć ņĢŖņĢśņ£╝ļ®░, MOG-ONņØĆ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüĻ▓Ćņé¼ņŚÉņä£ ņŗ£ņŗĀĻ▓Į ņŻ╝ļ│Ć ņŚ░ļČĆ ņĪ░ņ¦üņØś Ļ┤æļ▓öņ£äĒĢ£ ņŚ╝ņ”Ø ņåīĻ▓¼(perineural enhancement)ņØä ĒŖ╣ņ¦Ģņ£╝ļĪ£ ļ│Ė ņ”ØļĪĆņÖĆļŖö ĻĄ¼ļ│äļÉśļéś anti-MOG AbņŚÉ ļīĆĒĢ£ Ēśłņ▓ŁĒĢÖņĀü ĒÅēĻ░ĆĻ░Ć ņŗ£Ē¢ēļÉśņ¦Ć ņĢŖņĢśĻĖ░ņŚÉ MOG-ONņŚÉ ļīĆĒĢ£ ņÖäņĀä ļ░░ņĀ£Ļ░Ć ļČłĻ░ĆĒĢśņśĆļŗżļŖö ņĀÉņØä ļōż ņłś ņ׳ļŗż[12]. MOG AbļŖö AQP-4 AbĻ░Ć ņØīņä▒ņØĖ non-MS ONĻ│╝ ņŚ░Ļ┤ĆļÉśņ¢┤ ņ׳ņ£╝ļ®░, MOG-ONņØś Ļ▓ĮņÜ░ NMO-ONļ│┤ļŗż ņ×¼ļ░£ņØ┤ ļŹö ņ×”Ļ│Ā ņ┤łĻĖ░ ņŗ£ļĀźņØĆ ļé«ņØäņ¦ĆļØ╝ļÅä ņŗ£ļĀźņśłĒøäļŖö ņóŗļŗż[2,13,14]. Chen et al [14]ņØś ļ│┤Ļ│ĀņŚÉņä£ MOG-ON ļ░£ļ│æ ņ┤łĻĖ░ ņŗ£ ĒÅēĻĘĀ ņŗ£ļĀźņØĆ ņĢłņĀäņłśņ¦ĆņśĆņ£╝ļéś ņČöņĀü Ļ┤Ćņ░░ ņŗ£ 0.63ņ£╝ļĪ£ Ē¢źņāüļÉśņŚłļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļÅä ņĀäĒśĢņĀüņØĖ NMO-ONĻ│╝ ļŗżļź┤Ļ▓ī Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ņ╣śļŻī Ēøä ņŗ£ļĀźņØ┤ 1.0/0.8ļĪ£ ĒśĖņĀäļÉśņŚłļŗż. ņØ┤ņÖĆ Ļ░ÖņØĆ Ļ▓ĮņÜ░ anti-MOG Ab ĒśłņĢĪ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØ┤ ņ¦äļŗ©ņŚÉ ļŹö ļÅäņøĆņØ┤ ļÉśņŚłņØä Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż. ļśÉĒĢ£, ļŗżļ░£Ļ▓ĮĒÖöņ”Øņ£╝ļĪ£ņØś ĒÖĢņ¦äņØ┤ ņ¢┤ļĀżņÜ┤ ļ╣äņĀäĒśĢņĀüņØĖ Ļ▓ĮņÜ░, Palace et al [10]ņŚÉņä£ NMOSDņŚÉņä£ ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆĻ░Ć ņĀüņÜ®ļÉĀ Ļ▓ĮņÜ░ AQP-4 Ab ņłśņ╣śĻ░Ć ņāüņŖ╣ļÉśļŖö ņĀÉņØä ĒåĄĒĢ┤ ņØĖĒä░ĒÄśļĪĀ ļ▓ĀĒāĆ ņ╣śļŻī ņżæņŚÉļŖö ņ¦ĆņåŹņĀüņØĖ AQP-4 Ab ņČöņĀü Ļ┤Ćņ░░ņØ┤ ņ¦äļŗ©ņŚÉ ļÅäņøĆņØ┤ ļÉĀ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.
ņŗ£ņŗĀĻ▓ĮņŚ╝ņØś ņøÉņØĖņŚÉ ļö░ļØ╝ ĒŖ╣ņ¦ĢņĀüņØĖ ņ×äņāü ņåīĻ▓¼ņØ┤ ņĪ┤ņ×¼ĒĢ©ņŚÉļÅä MS-ONĻ│╝ NMOSD-ONņØä ņÖäņĀäĒ׳ Ļ░Éļ│äĒĢśļŖö Ļ▓āņØĆ ņ¢┤ļĀżņÜĖ ņłś ņ׳ļŗż[2,5]. ņ¦łĒÖśņØś ļ░£ļ│æ Ēøä ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņ┤¼ņśü ņŗ£ņĀÉņŚÉ ļö░ļØ╝ Ļ░ÖņØĆ ņ¦łĒÖśņØ┤ļØ╝ļÅä ĒÖśņ×Éļ¦łļŗż ņāüņØ┤ĒĢ£ ņśüņāü ņåīĻ▓¼ņØä ļ│┤ņØ╝ ņłś ņ׳ņ£╝ļ®░, Ļ░ü ņ¦łĒÖśļ¦łļŗż ĒĢŁņāü ņĀäĒśĢņĀüņØĖ ņ”ØņäĖņÖĆ ņåīĻ▓¼ņØä ļ│┤ņØ┤ļŖö Ļ▓āņØĆ ņĢäļŗłļŗż[2]. ļśÉĒĢ£ ĒÖ£ļ░£ĒĢ£ ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ┤ ļæÉ ņ¦łĒÖśņØś ņ░©ņØ┤ņĀÉņØ┤ ļŹöņÜ▒ ļ░ØĒśĆņ¦ĆĻ│Ā ņ׳ņ£╝ļéś, ļæÉ ņ¦łĒÖś ļ¬©ļæÉ ņ£Āļ│æļźĀņØ┤ ļé«Ļ│Ā ņĀäĒ¢źņĀü ņŚ░ĻĄ¼ļź╝ ņäżĻ│äĒĢśĻĖ░ ņ¢┤ļĀĄĻĖ░ ļĢīļ¼ĖņŚÉ ņĀĢĒÖĢĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ņĢäņ¦ü ļŗż ņØ┤ļżäņ¦Ćņ¦Ć ņĢŖņĢśļŗż[3,15].
ļ╣äņĀäĒśĢņĀüņØĖ ņ”ØņäĖļź╝ ļ│┤ņØ┤ļŖö ņ¢æņĢł ņŗ£ņŗĀĻ▓ĮņŚ╝ņØĆ ļŗżļ░£Ļ▓ĮĒÖöņ”ØņŚÉņä£ ļō£ļ¼Ė ĒśĢĒā£ņØ┤ļŗż. AQP-4 Ab, anti-MOG AbņÖĆ Ļ░ÖņØĆ ņ¦łļ│æĒŖ╣ņØ┤ĒĢŁņ▓┤Ļ▓Ćņé¼ņÖĆ ĒĢ©Ļ╗ś ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņØä ĒżĒĢ©ĒĢ£ ņ▓ĀņĀĆĒĢ£ ņ¦äļŗ© Ļ│╝ņĀĢņØä ĒåĄĒĢśņŚ¼ ņ£Āļ░£ Ļ░ĆļŖźĒĢ£ ļŗżņ¢æĒĢ£ ņøÉņØĖ ņ¦łĒÖśņØä Ļ░Éļ│ä ļ░░ņĀ£ĒĢśĻ│Ā ņĀĢĒÖĢĒĢ£ ņ╣śļŻīļź╝ ņĀüņÜ®ĒĢśļŖö Ļ▓āņØ┤ ņŗ£ļĀźņśłĒøä Ē¢źņāüņŚÉ ļÅäņøĆņØ┤ ļÉĀ Ļ▓āņØ┤ļŗż. ņČöĒøä ņāłļĪ£ņÜ┤ Ēśłņ▓ŁĒĢÖņĀü biomarkerņÖĆ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü ĻĖ░ļ▓ĢņØś ļ░£ļŗ¼ņØä ĒåĄĒĢśņŚ¼ Ļ░ü ņ¦łĒÖśņØś ĒŖ╣ņ¦ĢņĀüņØĖ ļ│æļ”¼ņāØĒā£ņŚÉ ļīĆĒĢ£ ņØ┤ĒĢ┤Ļ░Ć ļŹöņÜ▒ ĒĢäņÜöĒĢĀ Ļ▓āņØ┤ļŗż.
Figure┬Ā1.
A fundus photograph, retinal nerve fiber layer (RNFL) and ganglion cell complex (GCC) optical coherence tomography (OCT), and visual field test of the patient taken at the initial visit. (A) Fundus photography shows no disc swelling in both eyes. (B, C) RNFL and GCC OCT show no decreased thickness of RNFL and ganglion cell layer (GCL). (D) Humphrey field analyzer shows bitemporal hemianopsia. IPL = inner plexiform layer; OD = oculus dexter; OS = oculus sinister.

Figure┬Ā2.
Brain magnetic resonance imaging (MRI) and cervical spine MRI of the patient taken at the initial visit. (A) Brain MRI shows high signal intensities at optic chiasm and left retrobulbar segment of optic nerve (white arrow) in axial T2-flair weighted image. (B) Cervical spine MRI shows high extensive edematous bright foci at C2-C5 segment and medulla oblongata of the lower brain (dashed white circle) in sagittal T2-flair weighted image.
Figure┬Ā3.
A fundus photograph, ganglion cell complex (GCC) optical coherence tomography (OCT), and visual field test of the patient 1 month after treatment was completed. (A) Fundus photography shows no disc swelling in both eyes. (B) Ganglion cell layer (GCL) thickness was decreased in the GCC OCT in both eyes. (C) In Humphrey field analyzer, bitemporal hemianopsia shown at the initial visit improved. IPL = inner plexiform layer; OD = oculus dexter; OS = oculus sinister.

REFERENCES
2) Srikajon J, Siritho S, Ngamsombat C, et al. Differences in clinical features between optic neuritis in neuromyelitis optica spectrum disorders and in multiple sclerosis. Mult Scler J Exp Transl Clin 2018;4:2055217318791196.



3) Kim NH. Differential diagnosis between multiple sclerosis and neuromyelitis optica spectrum disorder. J Korean Neurol Assoc 2016;34:290-6.

4) Kang MH, Park KA. Comparison of optic neuritis with seropositive myelin oligodendrocyte glycoprotein antibody and seropositive neuromyelitis optica antibody. J Korean Ophthalmol Soc 2021;62:538-44.

6) Lana-Peixoto MA, Talim N. Neuromyelitis optica spectrum disorder and anti-MOG syndromes. Biomedicines 2019;7:42.



7) Piccolo L, Woodhall M, Tackley G, et al. Isolated new onset 'atypical' optic neuritis in the NMO clinic: serum antibodies, prognoses and diagnoses at follow-up. J Neurol 2016;263:370-9.


8) Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177-89.



9) Mealy MA, Whetstone A, Orman G, et al. Longitudinally extensive optic neuritis as an MRI biomarker distinguishes neuromyelitis optica from multiple sclerosis. J Neurol Sci 2015;355:59-63.



10) Palace J, Leite MI, Nairne A, Vincent A. Interferon beta treatment in neuromyelitis optica: increase in relapses and aquaporin 4 antibody titers. Arch Neurol 2010;67:1016-7.

11) Warabi Y, Matsumoto Y, Hayashi H. Interferon beta-1b exacerbates multiple sclerosis with severe optic nerve and spinal cord demyelination. J Neurol Sci 2007;252:57-61.


12) Kim SM, Kim SJ, Lee HJ, et al. Differential diagnosis of neuromyelitis optica spectrum disorders. Ther Adv Neurol Disord 2017;10:265-89.



13) Sato DK, Callegaro D, Lana-Peixoto MA, et al. Seronegative neuromyelitis optica spectrum--the challenges on disease definition and pathogenesis. Arq Neuropsiquiatr 2014;72:445-50.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,196 View
- 22 Download
- Related articles
-
Kimura Disease Presenting as Unilateral Proptosis2022 March;21(1)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print