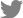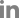|
 |
Abstract
Purpose
To investigate the clinical characteristics of patients clinically diagnosed with anti-GQ1b antibody syndrome.
Methods
From November 2005 to July 2019, we retrospectively reviewed the medical records of 52 patients diagnosed with Miller-Fisher syndrome, Bickerstaff brainstem encephalitis or anti-GQ1b antibody syndrome. Symptom including acute ophthalmoplegia, ataxia, hyporeflexia and other neurologic features were reviewed. Laboratory results including cerebrospinal fluid (CSF) analysis and anti-ganglioside antibodies were also analyzed.
Results
Among 52 patients, 40 were diagnosed with classic Miller-Fisher syndrome, 3 patients were Guillain-Barré syndrome with ophthalmoparesis, 1 patient was acute ophthalmoparesis without ataxia, 2 patients were acute ataxic neuropathy, and 6 patients were diagnosis with Bickerstaff brainstem encephalitis. Thirty five patients were male (67.3%), the mean age of onset was 39.3 ± 16.7 years, and average follow-up duration was 9.6 ± 15.9 months. Forty-four patients (84.6%) showed preceding infection, and upper respiratory infection was more common than gastrointestinal infection. Forty-nine patients (94.2%) showed ophthalmoplegia, 48 patients (92.3%) showed ataxia and hyporeflexia was presented in 43/51 patients (84.3%). Other than classic symptoms, dysarthria (21/52, 40.4%), dizziness (27/52, 51.9%), and paresthesia (23/52, 44.2%) was observed. Among 48 patients who underwent CSF analysis, 11 patients (22.9%) showed albumino-cytologic dissociation. Only 12 patients (23.1%) had positive anti-ganglioside antibodies.
Conclusions
Anti-GQ1b antibody syndrome is not easy to differentiate from other diseases, careful physical examination and history taking is necessary to make correct diagnosis. The recognition of accompanying symptoms and signs could facilitate early and exact diagnosis of anti-GQ1b antibody syndrome.
운동실조, 건반사 저하, 눈근육마비의 세 가지 주된 증상의 일부 혹은 모두를 나타내는 질환들과 이에 더해 다른 신경학적 이상이 동반되는 다양한 유사 아형 질환 환자들의 혈청에서 공통적으로 immunoglobulin G (IgG) 형의 항 GQ1b 항체가 증가되어 있는 것이 발견되며 항 GQ1b 항체증후군(anti-GQ1b antibody syndrome)이라는 개념이 생겨났다. 이에 대표적인 질환인 밀러-피셔증후군(Miller Fisher syndrome, MFS)은 운동실조, 무반사, 눈근육마비 3대 주증상을 나타내며 Collier [1]에 의해 1932년 길랑-바레증후군(Guillain Barré syndrome, GBS)의 변형으로 소개된 후, 1956년 Fisher [2]에 의해 독립된 질환으로 발표되었다. 또한 밀러-피셔가 발표하기 5년 전인 1951년 Bickerstaff and Cloake [3]에 의해 의식저하를 동반하며 눈근육마비와 운동실조증이 발생하는 중간 뇌병변으로 인한 뇌줄기염이 보고되었다. 이후 여러 아형들이 발견되었고, 여러 연구를 통해 항 GQ1b 항체가 운동실조, 무반사, 눈근육마비를 보이는 환자들에게 발견이 되었으며 추후 회복기에는 항체가 감소하였고 GBS 및 다발경화증 환자들에서는 이러한 항체가 보이지 않아 진단에 특이적인 항체로 보고되었다[4,5]. GBS로 발현하지만 눈근육마비를 같이 동반한 경우(GBS with ophthalmoparesis), MFS의 3대 주 증상 중 운동실조, 무반사를 동반하지 않고 눈근육마비가 주 증상으로 나타나는 경우(acute ophthalmoplegia without ataxia), 눈근육마비 없이 운동실조와 무반사만 나타나는 경우(acute ataxic neuropathy), 운동실조 및 눈근육마비를 가지면서 의식저하가 동반되는 경우(Bickerstaff brainstem encephalitis) 등을 항 GQ1b 항체증후군의 아형으로 볼 수 있다(Table 1). 또한 이들 환자에서 선행되는 상기도 감염 혹은 위장관 감염 후에 증상이 생기는 것 또한 중요한 진단의 단서이다[4].
안과의사들에게 MFS는 익숙한 진단명이나 비커스태프 뇌줄기염은 상대적으로 생소한 진단명이며 두 증후군이 비슷한 임상양상을 가지나 몇 가지 임상양상에서 차별점을 가지고 있고, 특히 후자에서는 의식저하 및 호흡곤란 등을 동반할 수 있어 혈장교환술 및 면역글로불린 치료를 해야 된다. 비커스태프 뇌줄기염에서는 건반사가 정상 또는 항진이 되는 경우도 있으며, 뇌실 맨 아래 구역을 침범하여 심한 오심, 구토 증상을 일으켜 시신경척수염 등으로 오인되고 다른 탈수초성 질환이나 뇌혈관질환과 감별진단이 필요한 경우도 있다[5]. 따라서, 항 GQ1b 항체증후군을 진단하는 데 있어 항 GQ1b 항체가 검출되는 경우는 진단적인 특이도가 있으나, 진단 기준이 되는 증상의 다양한 조합들이 있을 때도 진단이 가능하며, 여러 아형들 사이에 뚜렷한 경계가 없는 것이 특징이다. 따라서, 흔히 안구운동장애 및 사시가 동반되므로 이를 진단하는 데 있어 안과의사 역할이 중요하며 MFS를 비롯한 항 GQ1b 항체증후군에 대한 안과의사의 이해가 필요할 것으로 생각된다. 따라서 본 연구에서는 항 GQ1b 항체증후군의 임상적 특성을 후향적으로 조사하여 나타나는 다양한 임상양상을 비교해보고자 한다.
2005년 11월부터 2019년 7월까지 강남세브란스병원(n=20) 및 신촌세브란스병원(n=32) 내원한 환자들 중 운동 실조 또는 건반사 저하, 급성 안구운동마비를 보이며 다른 감별질환이 진단에서 배제되어 MFS, 비커스태프 뇌줄기염 혹은 항 GQ1b 항체증후군으로 임상적으로 진단된 환자들 52명의 의무기록을 후향적으로 조사하였다. 본 연구는 모든 과정에서 헬싱키선언(Declaration of Helsinki)을 준수하였으며, 연세대학교 의과대학 세브란스병원 임상시험심위원회(Institutional Review Board)의 승인을 얻었다(승인 번호: 3-2019-0380). 항 GQ1b 항체증후군의 진단은 최근의 GBS classification group의 진단 기준으로 사용하였으며, 항 GQ1b 항체증후군 아형의 분류는 Table 1에 제시하였다[6]. 감별 진단으로 뇌자기공명영상에서 뇌줄기 경색을 배제하였으며, 반복신경자극검사와 아세틸콜린 수용체항체검사 결과 모두 음성으로 중증근무력증을, 알코올 섭취력, 건강 상태 평가 및 병력 청취를 통하여 베르니케 뇌병증, 보툴리누스중독증의 가능성을 배제하였으며, 의심이 되는 경우 비타민 B1, B6, B12 수치를 조사하여 정상 수치임을 확인하였다. 눈근육마비 없이 사지근육약화로 GBS로 진단된 경우도 제외하였다. 항 GQ1b 항체증후군에서 선행하는 감염질환의 종류를 확인하였으며, 눈근육마비, 복시, 내안근 마비, 안검하수, 운동실조, 건반사 저하, 구음장애 진료기록을 분석하였다. 또한, 발병 연령, 감염 후 증상이 생겼을 때까지 기간, 다른 뇌신경 침범 여부, 뇌척수액검사 및 항 강글리오시드 항체를 비교 분석하였으며, 항 GQ1b 항체증후군으로 진단받은 환자들이 각각의 증상을 갖고 있는 비율을 비교 분석하였다. 뇌척수액검사에서 뇌척수액단백세포해리는 세포의 수가 증가하지 않음에도 단백질의 수치가 증가하였을 때로 정의하였으며, 정상 레벨은 세포 수는 <6/μL, 단백질 수치는 45 mg/dL를 기준으로 하였다. 항 강글리오시드 효소면역측정법(enzyme-linked immunosorbent assay, ELISA)으로 외부 수탁검사로 서울의과학연구소(SCL, Yongin, Korea) 혹은 미국 Mayo clinic (Rochester, MN, USA)에 의뢰되어 시행되었으며, 일부 환자의 경우 동아대학교 의과대학 신경과로 검체를 보내 검사가 시행되었다. 통계방법은 Chi-square, Fisher exact test가 사용되었고 통계프로그램은 STATA software 16.1 (StataCorp LLC, College Station, TX, USA)가 이용되었다.
항 GQ1b 항체증후군으로 진단받은 52명의 환자들 중 40명(76.9%)은 MFS였으며 3명(5.7%)은 눈근육마비가 동반된 GBS 1명(1.9%)은 운동실조가 동반되지 않은 급성 눈근육마비, 2명(3.9%)은 눈근육마비가 동반되지 않은 급성운동실조신경병증 6명(11.5%)은 비커스태프 뇌줄기염으로 진단되었다(Table 2). 선행된 감염 증상은 52명 중 44명(84.6%)에서 나타났으며, 상기도 감염 증상(28명, 53.9%), 위장관 감염 증상(15명, 28.9%)의 비율을 나타내며 상기도 감염 선행이 더 많았으며, 3명은 두 감염이 복합되어 있었다.
임상증상 중 안구운동장애는 49명(94.2%), 복시가 47명(90.4%)의 환자에서 있었으며, 복시가 없는 5명 중 2명은 급성 운동실조 신경병증, 2명은 MFS, 1명은 비커스태프 뇌줄기염이었다. 운동실조는 48명(92.3%)에서 관찰되었으며, 건반사 저하는 MFS로 진단된 1명을 제외한 51명에서 검사가 되었으며 43명(84.3%)에서 존재하였다. 52명 중 22명(42.3%)에서 안검하수, 10명(16.1%)에서 동공 침범을 확인할 수 있었다. 급성 운동실조 신경병증으로 진단된 환자들에서는 안검하수, 동공마비의 증상을 확인할 수 없었으며, 운동실조가 동반되지 않은 급성 눈근육마비 환자 1명에서는 안검하수와 동공마비가 모두 관찰되었다. 눈근육마비가 동반된 GBS와 운동실조가 동반되지 않은 급성 눈근육마비군은 눈근육마비와 함께 복시를 100% 나타내고 있었고, MFS의 경우 38명(95%)에서 복시를 나타내며 눈근육마비는 모두에서 관찰되었다. 비커스태프 뇌줄기염의 경우 복시와 눈근육마비 모두 5명(83%)에서(complete 1명, incomplete 4명) 확인되었다. 제일눈위치에서 사시각이 없는 경우는 21명이었으며, 내사시가 22명으로 가장 많은 빈도로 관찰되었고, 수평과 수직사시가 같이 동반된 경우 6명, 외사시는 2명, 수직사시는 1명에서 관찰되었다.
전형적인 증상 외에 구음장애를 동반한 구마비는 21명(40.4%)에서 관찰되었으며, 비커스태프 뇌줄기염에서 가장 높은 비율(5명, 83.3%)로 확인되었다. 눈근육마비가 동반된 GBS로 진단된 3명 모두에서 인공호흡기 치료가 필요하였고, 비커스태프 뇌줄기염으로 진단된 6명 중 2명에서 인공호흡기 치료가 필요하였다. 한편, 뇌척수액 단백세포해리는 뇌척수액검사가 진행된 48명 중 11명(22.9%)에서 확인할 수 있었고, 항 강글리오시드 항체는 52명의 환자들 중 12명(23.1%)에서 검출되었다. GQ1b 항체 이외의 항 강글리오시드 항체가 발견된 경우로는 눈근육마비가 동반된 GBS 중 1명에서 항 GD1b IgG 항체 양성이었으며, MFS 중 2명에서 각각 항 GD1b IgM 및 항 GM1 IgM이 양성이었으며, 항 GQ1b IgG 항체는 관찰되지 않았다. 이 두 명의 환자에서 사지위약감은 없었으며 근력도 정상이었다. 항 GQ1b IgG 항체 양성은 8명이었으며, 항 GQ1b IgG 항체가 양성인 8명 중에서 3명은 항 GT1a IgG 항체가 같이 양성이었고, 두 항체 모두 양성인 3명은 구마비가 동반되어 있었다. 또한, MFS 1명에서는 항 GT1a IgG만 양성이었으며, 이 환자 역시 구마비가 동반되었다. 뇌자기공명영상에서 뇌신경의 조영증가가 관찰된 경우는 검사를 시행한 48명 중 7명(14.6%)으로 확인되었다. 치료는 고용량 스테로이드 정맥주사 투여군 11명(21.5%), 면역글로불린치료 24명(46.2%), 8명(15.4%)은 두 가지의 치료를 함께 시행 받았다.
32세 여자 환자가 내원 3일 전부터 시작된 하지저림 현상, 운동실조, 구음장애, 양측사지 위약감을 주소로 응급실에 내원하였다. 임신 36주의 산모였으며 내원 2주 전 위장관 감염 병력이 있었다. 내원하여 시행한 검사상 건반사 항진 소견이 있었고 의식저하가 심해져 응급 제왕절개술을 시행하였으며, 인공호흡기 치료를 하였다. 안과 협진이 의뢰되어 시행된 안과적 검사에서는 안검하수, 눈근육마비, 동공 확대 소견이 관찰되었다(Fig. 1A). 항 GQ1b 항체를 포함한 혈청검사에서 항체양성 소견은 관찰되지 않았다. 정맥면역글로불린 치료 후 점차 호전되는 양상을 보여 발병 3개월 후에는 내사시가 남아있지만, 6개월 후에는 완전히 호전되었다(Fig. 1B). 환자는 운동실조, 건반사 항진, 의식저하, 완전 눈근육마비 등의 증상으로 비커스태프 뇌줄기염으로 진단되었다.
24세 남자 환자가 내원 하루 전부터 우안 안검하수 및 구음장애가 생겨 내원하였다. 뇌 magnetic resonance imaging & magnetic resonance angiography상 정상이었으며, 내원 8일 전부터 설사, 복통이 있었다. 우안 동공은 산대되어 있었으며, 보행실조가 동반되었다. 심부건반사는 정상이었다. 우안 상전 -4, 하전 2-, 내전 4-의 안구운동장애가 관찰되었다(Fig. 2A-C). 뇌척수액검사상 세포단백해리는 없었으며, 항체검사상 anti-GQ1b IgG 및 anti-GT1a IgG 양성이었다. 스테로이드 정맥주사 치료를 하였으며, 환자는 2달 후 증상이 완전히 호전되었다(Fig. 2D).
본 연구에서 운동실조, 건반사저하, 눈근육마비 3대 주증상을 갖고 있다고 잘 알려진 MFS는 실제 임상에서 세 가지 임상증상 중 일부만 가지고 있는 경우가 많았으며, 의식 저하와 척수로 증상을 가지는 비커스태프 뇌줄기염, 사지마비가 동반되는 MFS-GBS 등으로 추후 최종 진단이 내려짐을 알 수 있었다. 본 연구 결과에서 대상자 62명 중 40명이 전형적인 MFS, 3명이 눈근육마비가 동반된 GBS, 1명이 운동실조가 동반되지 않은 급성 눈근육마비, 6명이 비커스태프 뇌줄기염으로 진단되었다. 따라서, 급성 안구운동장애로 내원하는 환자들에서 일부는 운동실조를 동반하지 않을 수도 있고, 사지 허약감 및 의식 저하가 동반될 수 있으므로 자세한 문진과 진찰이 필요할 것으로 생각된다.
MFS의 세 가지 대표 증상 중 눈근육마비는 다양한 양상으로 확인된다. 양측성 완전마비로 나타날 수도 있으며 불완전마비 혹은 비대칭적인 눈근육마비로 확인되기도 한다. 본 연구 결과에 따르면 운동실조가 동반되지 않은 급성 눈근육마비로 진단된 1명에서 나타난 눈근육마비는 양측성으로 나타났으며, 다른 진단군에서는 양측성과 편측성의 비율이 비슷하게 확인되었다. 또한, 눈근육마비가 동반된 GBS의 경우 눈근육마비가 나타난 3명 모두 완전마비의 양상을 보였다. 뇌척수액에서 뇌척수액단백세포해리는 모든 진단군에서 50% 이하의 확률로 확인되었으며, MFS군은 7명(18.4%), 비커스태프 뇌줄기염은 2명(33.3%)에서 관찰되었다. 이는 MFS 환자의 37%, 비커스태프 뇌줄기염 환자의 25%에서 증상 발생 첫 주에 뇌척수액 단백세포해리를 확인할 수 있다고 한 기존 연구 결과와 비슷한 수치이다[7].
현재까지 발표된 연구들에 의하면 MFS이 말초신경계 증상이 뚜렷한 데에 비해 비커스태프 뇌줄기염은 중추신경계의 증상이 뚜렷한 것으로 알려져 있다. 의식장애는 대표적인 비커스태프 뇌줄기염의 진단 기준으로 여겨지고 있고 비커스태프 뇌줄기염 환자들의 의식장애 정도는 다양하며, 건반사 항진 또한 비커스태프 뇌줄기염의 진단 기준으로 제시되는데, 이것은 중추신경계 기능 억제에 의하여 ‘upper motor neuron lesion sign’으로 조절되어야 할 건반사가 오히려 항진되는 것으로 설명할 수 있다. 항 GQ1b 항체가 중추신경계를 침범할 수 있는 가설을 뒷받침하는 것은 비커스태프 뇌줄기염 환자의 혈청이 혈액-뇌 장벽을 파괴할 수 있음을 증명한 실험과 혈액-뇌 장벽이 존재하지 않는 구역인 망상활성계의 침범이 가능하다는 가설 등이 있다[8,9]. 따라서, MFS와 유사한 임상양상을 보이면서 의식저하 혹은 건반사 항진이 동반되는 경우 비커스태프 뇌줄기염을 의심하고 인공호흡기치료 등이 필요할 수 있으므로 안과의사가 처음 환자를 진찰할 때 이러한 응급 상황들이 올 수 있음을 인지하여야 할 것으로 생각한다.
하지만, MFS 환자의 혈청에서 항소뇌항체가 발견되거나[10] fluorodeoxyglucose-positron emission tomography 연구에서 소뇌나 뇌간의 대사 항진이 확인된 연구에서 보듯이[11], MFS의 증상을 유발하는 염증이 말초신경계와 중추신경계 모두를 침범하는 것의 근거가 될 수 있으며, MFS 환자의 뇌자기공명영상에서 중뇌, 소뇌, 중간소뇌다리에 이상을 보였던 경우 또한 중추신경계 침범이 MFS과 전혀 별개의 발병 기전이 아님을 확인할 수 있다[12]. 실제로 본 연구에서도 자기공명영상에서 뇌신경의 조영증가가 확인된 비율이 비커스태프 뇌줄기염에서 20%로 가장 높았고, MFS에서 16.2%로 그 뒤를 따랐다. 즉, 비커스태프 뇌줄기염과 MFS는 임상증상, 검사실 소견, 발병 기전 등 많은 것을 공유하고 있음을 알 수 있다. 또한, GBS에서는 주로 GD1a, GD1b, GM1 항체가 연관이 되어 있다고 알려져 있으나 약 9-10%의 GBS 환자에서 항 GT1a와 항 GQ1b 항체가 양성을 나타내며 이런 환자들에서 눈근육마비, 안면마비가 흔하게 발견된다[13]. 따라서, 중추신경계와 말초신경계 중 어떤 장소에 면역 반응이 주로 일어나느냐에 따라 주요 증상이 달라질 뿐, 병태생리를 공유하는 하나의 질환 스펙트럼임을 확인할 수 있었다.
눈근육마비를 동반한 MFS 환자의 90% 이상에서 항 GQ1b 항체가 양성으로 나타나고[14], 정상 대조군에서는 거의 검출되지 않아 MFS 진단에 항 GQ1b 항체가 민감도와 특이도가 매우 높은 진단적 표지자로 평가 받아왔다. 비커스태프 뇌줄기염에서도 60% 이상에서 항 GQ1b 항체가 발견되면서 MFS와 함께 항 GQ1b 항체증후군으로 명명되고 있지만[15-17], 실제 본 연구에서는 62명 중 12명 즉, 19.4%의 환자에서만 항 강글리오시드 항체가 양성으로 확인되었다. 본 연구에서는 항 강글리오시드 항체에 대한 검사가 일부 환자에서 증상 시작 후 2-3주 지난 시점에서 시행되었으며, 외부업체 ELISA의 낮은 민감도가 항 GQ1b 항체 양성률에 영향을 끼쳤을 것으로 생각된다. 또한, 4명의 환자에서는 동아대학교 의과대학 신경과로 검체를 보냈으나 결과를 못 받은 경우도 있었다. 항체 간 구조적 유사성, 교차반응 등이 ELISA의 한계를 나타내지만, 이는 향후 연구를 통해서 검사의 질적 수준을 올릴 수 있는 방안을 모색하여야 될 것으로 생각한다[18]. 현재, 외주업체에서 시행되는 항체검사는 각각 IgG 및 IgM type으로 8가지 항 강글리오시드 항체(GM1, GM2, GD1a, GD1b, GD3, GT1a, GT1b, GQ1b)와 일부 중요한 복합 항체에 대해 시행되고 있으며, 본 연구 대상자 중 항 GQ1b 외에 강글리오시드 항체가 검출된 경우는 항 GT1a, 항 GD1b, 항 GM1 등이 있다. GQ1b 강글리오시드와 GT1a 강글리오시드는 구조적으로 서로 유사하며 두 강글리오시드에 반응하는 항체는 모두 눈운동마비와 밀접한 연관이 있다고 나와있고 눈운동마비를 동반한 MFS에서 높은 빈도로 발견된다. 또한, 항 GT1a 항체가 존재할 때는 구마비가 흔히 동반됨을 인지하여야 한다[18].
한편, 본 연구에서 후향적 연구 분석으로 2개의 기관에서 환자를 분석한 것이 한계점으로 생각된다. 또한, 항 강글리오시드 항체 검사의 민감도가 낮았던 점이 연구의 한계점으로 생각된다. 또한, 항 GQ1b 항체증후군 환자들 중에서 주로 신경과만을 내원한 환자들도 있어 정확한 눈근육운동 검사, 사시량 측정이 이뤄지지 못하여 정량적인 눈근육마비의 정도를 분석하지 못하였다. 또한 질환의 특성상 치료 없이도 2-3개월 정도에 자연 회복하는 질환이기 때문에, 안과 혹은 신경과 내원 후 정기적인 추적 관찰이 되지 않아 환자들의 회복 양상을 파악하기 어려웠다.
본 연구를 통해서 항 GQ1b 항체증후군으로 통칭되는 여러 진단군들이 전형적인 MFS 형태로 나타날 수도 있지만, 비커스태프 뇌줄기염 혹은 눈근육마비가 동반된 GBS 같이 다양한 임상증상을 나타냄을 확인할 수 있었다. 또한, 환자가 항 GQ1b 항체증후군의 가장 대표적인 증상인 급성 안운동장애를 주 호소로 병원에 내원하였을 때, 항 GQ1b 항체증후군을 포함한 중증근무력증, 3번 신경마비, 갑상선안 병증, 베르니케 뇌병증, 보툴리누스중독증 등을 감별하여 되는데, 이상감각, 어지러움, 구마비, 동공침범 등의 증상을 추가적으로 확인하여 정확한 진단을 할 수 있음을 확인할 수 있었다. 향후 더 많은 연구 대상자 수를 바탕으로 질환의 경과, 항체의 발현 정도, 임상양상, 치료 경과를 비교하는 연구가 필요할 것으로 생각된다.
Figure 1.
External photographs of 32-year-old female with Bickerstaff brainstem encephalitis. This 36-weeks pregnant female presented to the emergency department with paresthesia, ataxia, weakness of extremities, and dysarthria. Her mental status was drowsy, and hyperreflexia was noted in deep tendon reflex. Complete ophthalmoplegia, bilateral ptosis and mydriasis were also noted. Intubation was done, and emergent cesarean section was completed. Brain magnetic resonance imaging was normal, and GQ1b antibody was negative. (A) External ophthalmoplegia was noted in all direction gaze (photograph shown in left gaze) at initial presentation. (B) The ophthalmoplegia was completely resolved at 6 months after onset.
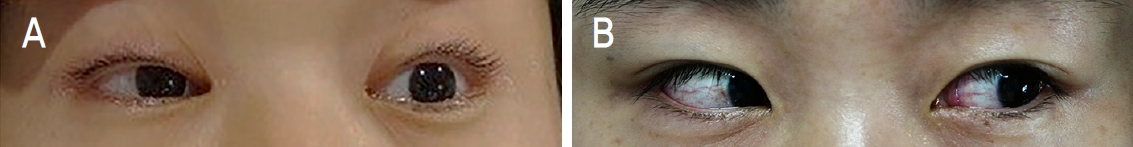
Figure 2.
External photograph of 24-year-old male who presented with ptosis, diplopia and dysarthria. The patients presented to the emergency department after suffering 1 day of multiple symptoms, including ptosis, double vision, slurred speech and difficulty with his coordination. He had history of severe diarrhea lasted for 5 days, and the symptom had stopped 3 days previously. He was alerted and fully oriented. (A-C) There was weakness with medial, up, and down gaze on the right eye. The pupil in the right eye was mid-dilated, and magnetic resonance imaging with angiography showed normal. Strength was 5/5 throughout. GQ1b IgG and GT1a IgG was positive, suggestive of Miller-Fisher syndrome. (D) He was completely recovered after 2 months.

Table 1.
Differential diagnosis of a patient with anti-GQ1b antibody syndrome
| Disease | Extraocular motility abnormality | Lid abnormality (ptosis) | Ataxia | Areflexia | Other abnormality | Anti-ganglioside antibody |
|---|---|---|---|---|---|---|
| Miller-Fisher syndrome | Yes | May be present | Yes | Yes | Facial weakness | >90% |
| Guillain-Barré syndrome with ophthalmoparesis | Yes | May be present | May be present | May be present | Flaccid paralysis* | Up to 83% with ophthalmoplegia |
| Bulbar weakness | ||||||
| Sensory loss | ||||||
| Acute ophthalmoplegia without ataxia | Yes | May be present | Yes | No | No | 100% (required for diagnosis) |
| Acute ataxic neuropathy | No | No | Yes | Yes | No | More often GD1b |
| Bickerstaff brainstem encephalitis | Yes | May be present | Yes | Sometimes, hyper-reflexia or normoactive | Pyramidal weakness | Up to 68% |
| Altered level of consciousness* |
Table 2.
Clinical characteristics of anti-GQ1b antibody syndrome according to its subtype
| Miller-Fisher syndrome (n = 40) | GBS with ophthalmoparesis (n = 3) | Acute ophthalmoparesis without ataxia (n = 1) | Acute ataxic neuropathy (n = 2) | Bickerstaff brainstem encephalitis (n = 6) | |
|---|---|---|---|---|---|
| Male:female (male ratio) | 27:13 (67.5) | 2:1 (66.7) | 0:1 (0) | 1:1 (50.0) | 5:1 (83.3) |
| Onset age (years) | 39.5 ± 17.6 | 39.9 ± 22.7 | 47.3 | 43.9 ± 23.3 | 34.7 ± 8.4 |
| Previous infections | URI: 22 (55.0) | URI: 2 (66.7) | 0 | URI: 1 (50.0) | URI: 3 (50.0) |
| GI: 12 (30.0) | GI: 1 (33.3) | GI: 2 (33.3) | |||
| Combined: 2 (5.0) | Combined: 1 (16.7) | ||||
| Interval between infections and onset date (days) | 12.9 ± 15.1 (2-90) | 7.3 ± 6.1 (2-14) | Not avaiable | 10.0 | 7.5 ± 3.9 (3-14) |
| Ataxia | 37 (92.5) | 3 (100) | 0 | 2 (100) | 6 (100) |
| Hyporeflexia | 34 (85.0) | 3 (100) | 0 | 2 (100) | 4 (66.7) |
| Ptosis | 17 (42.5) | 1 (33.3) | 1 (100) | 0 | 3 (50.0) |
| Pupil involvement | 7 (17.5) | 0 | 1 (100) | 0 | 2 (33.3) |
| Diplopia | 38 (95.0) | 3 (100) | 1 (100) | 0 | 5 (83.3) |
| Ophthalmoparesis (n) | Unilateral = 17 | Unilateral = 2 | Bilateral = 1 | None = 2 | None = 1 |
| Bilateral = 23* | Bilateral = 1 | Unilateral = 3 | |||
| Bilateral = 2 | |||||
| Complete of incomplete ophthalmoplegia (n) | Complete = 10 | Complete = 3 | Complete = 1 | Complete = 0 | Complete = 1 |
| Incomplete = 30 | Incomplete = 0 | Incomplete = 0 | Incomplete = 4 | ||
| Dysarthria | 13 (32.5) | 2 (66.7) | 0 | 1 (50.0) | 5 (83.3) |
| Paresthesia | 18 (45.0) | 1 (33.3) | 0 | 2 (100) | 2 (33.3) |
| Dizziness | 21 (52.5) | 1 (33.3) | 1 (100) | 1 (50.0) | 3 (50.0) |
| Ventilator care | 0 | 3 (100) | 0 | 0 | 2 (33.0) |
| Albuminocytologic dissociation | 7/38 (18.4) | 1/2 (50.0) | Not done | 1/2 (50.0) | 2/6 (33.3) |
| Anti-ganglioside Ab (anti GQ1b IgG = 8/12, 66.7%) | 7 (17.5) (Anti GQ1b IgG = 4) | 1 (33.3) | 1 (100) (Anti GQ1b IgG = 1) | 0 | 3 (50.0) (Anti GQ1b IgG = 3) |
| MRI enhancement on cranial nerve | 6/37 (16.2) | 0/3 | 0 | 0/2 | 1/5 (20.0) |
Values are presented as mean ± standard deviation (range) or number (%).
GBS = Guillain-Barré syndrome; URI = upper respiratory infection; GI = gastrointestinal infection; Ab = antibody; IgG = immunoglobulin G; MRI = magnetic resonance imaging.
REFERENCES
1) Collier J. Peripheral Neuritis. The Morrison Lectures, 1932, Delivered before the Royal College of Physicians of Edinburgh, May 1932. Edinb Med J 1932;39:601-18.


2) Fisher M. An unusual variant of acute idiopathic polyneuritis (syndrome of ophthalmoplegia, ataxia and areflexia). N Engl J Med 1956;255:57-65.


4) Odaka M, Yuki N, Hirata K. Anti-GQ1b IgG antibody syndrome: clinical and immunological range. J Neurol Neurosurg Psychiatry 2001;70:50-5.



5) Bickerstaff ER. Brain-stem encephalitis; further observations on a grave syndrome with benign prognosis. Br Med J 1957;1:1384-7.


6) Wakerley BR, Uncini A, Yuki N, the GBS Classification Group. Guillain-Barré and Miller Fisher syndromes--new diagnostic classification. Nat Rev Neurol 2014;10:537-44.


7) Ito M, Matsuno K, Sakumoto Y, et al. Ataxic Guillain-Barré syndrome and acute sensory ataxic neuropathy form a continuous spectrum. J Neurol Neurosurg Psychiatry 2011;82:294-9.

8) Saito K, Shimizu F, Koga M, et al. Blood-brain barrier destruction determines Fisher/Bickerstaff clinical phenotypes: an in vitro study. J Neurol Neurosurg Psychiatry 2013;84:756-65.


9) Faraci FM, Choi J, Baumbach GL, et al. Microcirculation of the area postrema. Permeability and vascular responses. Circ Res 1989;65:417-25.

10) Inoue A, Koh C, Iwahashi T. Detection of serum anticerebellar antibodies in patients with Miller Fisher syndrome. Eur Neurol 1999;42:230-4.


11) Kim YK, Kim JS, Jeong SH, et al. Cerebral glucose metabolism in Fisher syndrome. J Neurol Neurosurg Psychiatry 2009;80:512-7.


12) Ito M, Kuwabara S, Odaka M, et al. Bickerstaff's brainstem encephalitis and Fisher syndrome form a continuous spectrum: clinical analysis of 581 cases. J Neurol 2008;255:674-82.


13) Koga M, Yoshino H, Morimatsu M, Yuki N. Anti-GT1a IgG in Guillain-Barré syndrome. J Neurol Neurosurg Psychiatry 2002;72:767-71.


14) Lo YL. Clinical and immunological spectrum of the Miller Fisher syndrome. Muscle Nerve 2007;36:615-27.


15) Suzuki T, Chiba A, Kusunoki S, et al. Anti-GQ1b ganglioside antibody and ophthalmoplegia of undetermined cause. Br J Ophthalmol 1998;82:916-8.



16) Chiba A, Kusunoki S, Shimizu T, Kanazawa I. Serum IgG antibody to ganglioside GQ1b is a possible marker of Miller Fisher syndrome. Ann Neurol 1992;31:677-9.


17) Koo DL, Park GH, Kim HT, et al. Acute monocular ophthalmoplegia associated with anti-GQ1b IgG antibody. J Korean Neurol Assoc 2004;22:663-5.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Download Citation
Download Citation Print
Print