유리체절제술과 함께 시행한 백내장수술에서 굴절오차 분석
Refractive Outcomes after Primary Vitrectomy Combined with Cataract Surgery
Article information
Trans Abstract
Purpose
To evaluate the tendency of refractive prediction error and to examine factors that affect the refractive changes after combined vitrectomy and cataract surgery.
Methods
We retrospectively reviewed demographic and clinical data, including axial length, intraocular pressure (IOP), preoperative anterior chamber depth, target refraction, preoperative refraction, postoperative refraction, keratometry, and refractive prediction error (the difference between postoperative and target refraction) of a retinal detachment (RD) group (28 eyes) and an epiretinal membrane (ERM) group (82 eyes). Both groups underwent combined vitrectomy and cataract surgery.
Results
The refractive prediction error with myopic shift was evident in total patients (-0.85 ± 0.85 D, p < 0.001), the RD group (-0.92 ± 1.13 D, p = 0.007), and the ERM group (-0.83 ± 0.78 D, p < 0.001). There was no significant difference between preoperative and postoperative keratometry in the two groups (p = 0.742 and 0.500, respectively). The preoperative IOP of the affected eye was significantly lower than that of the unaffected eye in the RD group (p = 0.012). In multivariate regression analysis, preoperative axial length was significantly correlated with the refractive prediction error in both the RD (β = 0.189, p = 0.036) and ERM (β = 0.689, p < 0.001) groups. Age, IOP, and preoperative visual acuity were not significantly associated with the refractive prediction error.
Conclusions
A significant myopic shift was observed in the RD and ERM groups after combined vitrectomy and cataract surgery with gas tamponade. The preoperative axial length was significantly correlated with the refractive prediction error in both groups.
최근 유수정체안에서 유리체망막 질환에 대한 유리체절제술을 시행할 때 유리체절제술과 백내장 병합수술이 많이 시행되고 있다. 이는 수술 당시에 환자가 이미 백내장을 가지고 있는 경우도 많고, 유리체절제술 후 백내장이 빨리 진행되는 합병증이 있을 수 있으므로 병합수술을 고려하게 되기 때문이다. 유리체절제술과 백내장수술을 동시에 할 경우 백내장 제거로 인한 시야 확보로 주변부 망막에 대한 접근이 용이하고 한 번의 수술로 빠른 시력회복을 가져올 수 있다는 장점이 있으며, 추가 수술에 필요한 시간과 비용을 절감할 수 있다[1-3]. 이러한 장점에도 불구하고, 병합수술 시행 시 수술 시간이 길어짐에 따라 수술 중 합병증 발생 위험의 증가나 수술 후 목표 굴절치의 오차, 후낭혼탁, 근시 이행, 홍채후유착 등이 잘 생길 수 있다고 보고되어 있다[4,5].
유리체절제술과 백내장 병합수술에서 술자의 목표는 유리체망막 병변의 치료와 함께 예상했던 굴절력과 실제 술 후 굴절력의 오차를 최대한 적게 하여 환자의 술 후 최대교정시력을 증가시키는 것이다. 백내장수술을 단독으로 시행하는 경우, 인공수정체를 넣었을 때 목표 굴절치와 실제 결과값에 대한 연구가 여러 공식을 통하여 정립되어 있다. 그러나, 유리체절제술과 병합하여 시행한 백내장수술의 경우 많은 변수가 술 후 굴절력에 영향을 줄 수 있기 때문에 이에 대해서 아직 많은 연구들이 진행 중이며 연구자마다 다양한 결과를 보고하고 있다[6-13]. 백내장 단독수술에 비하여 유리체절제술과 병합수술을 하였을 때 -0.5 diopter (D)의 근시편위(myopic shift)를 보였다는 연구가 있었고[6,7], 긴 안축장을 가지거나 수술 전 시력이 좋지 않을 때, 수술 전 황반을 침범한 망막박리가 있을 때 주로 근시편위가 생긴다는 보고도 있었다[8]. 망막박리와 망막앞막에 대하여 백내장수술을 하지 않고 유리체절제술만 한 경우에도 두 그룹에서 모두 근시편위를 보였으며 이는 핵경화백내장의 진행과 유리체절제술 자체에 의한 것이라는 연구도 있었다[9]. 유리체절제술 시 가스 주입을 한 군과 하지 않은 군을 비교하였을 때 가스를 주입한 군만 근시편위를 보였고 이는 가스에 의해 인공수정체가 앞으로 밀린 것이 원인이라는 가설도 있었지만[7,14], 이미 인공수정체를 가지고 있는 환자에서 유리체절제술 후 가스를 주입하였을 때 전방깊이를 측정하였더니 줄어들지 않았다고 보고한 연구도 있었다[10].
안압 또한 백내장수술 후 굴절력에 영향을 줄 수 있는데, 과거 섬유주절제술을 한 환자들에서 백내장수술을 진행하였을 때 안압이 2 mmHg 증가하면 -0.36 D의 굴절오차를 보였다[11]. 이에 기초하여 국내에서 진행된 연구 중에 망막 박리가 있는 쪽 안구가 안압이 낮지만 유리체절제술과 백내장수술을 동시에 진행한 후 안압이 정상화되면서 안축장을 증가시키고 굴절오차가 근시성 변화를 보였다는 연구가 있다[12,13]. 하지만 이 연구는 A-scan이라는 접촉식 초음파를 사용하여 안축장을 측정하였기 때문에 함입 편향(indentation bias)이 굴절력 측정에 영향을 주었을 것으로 생각되며, 대조군에 망막박리를 제외한 여러 유리체망막질환을 포함시켜 분석하였기 때문에 질병 각각에 대해서는 결과가 구체화되지 않았다.
본 연구는 유리체절제술과 백내장 병합수술 이후의 굴절 오차에 대해 알아보기 위해 기존 연구의 한계점을 보완하고자 계획하였다. 본 연구에서는 비접촉식 생체계측기인 IOL master로 안축장을 측정하여 접촉식 초음파 측정 방식에 의한 오차를 제거하였으며, 연구 대상을 망막박리와 망막앞막이라는 특정 질환으로 제한시켰다. 또한, 유리체절제술과 백내장 병합수술을 하였을 때의 수술 후 굴절력 예측 오차를 비교하였고, 이에 영향을 주는 요인을 분석하고자 하였다.
대상과 방법
본 연구는 2013년 9월부터 2017년 12월까지 서울성모병원에서 유리체절제술과 백내장 병합수술을 시행 받은 환자 중 술 후 12개월 이상 추적 관찰이 가능하였던 환자를 대상으로 후향적 의무기록 분석을 시행하였다. 망막박리 또는 망막앞막으로 유리체절제술과 백내장 병합수술을 받은 환자가 연구에 포함되었고, 대상자 중 굴절수술을 포함한 안과적 수술 과거력, 각막혼탁, 선천적인 안구의 이상, 노인성 황반변성을 포함한 다른 유리체망막질환이 동반된 경우, 심한 매체혼탁, 녹내장이 있는 경우, 수술 중 후낭파열 등의 예상치 못한 합병증이 발생한 경우는 제외하였다. 망막박리는 황반부를 침범하였을 경우 안축장 측정에서 오차가 발생할 수 있기 때문에 황반부를 침범하지 않은 열공망막박리만을 포함하였고, 장액망막박리, 견인망막박리는 제외하였다. 본 연구는 헬싱키선언에 입각하여 본원의 임상시험연구윤리심의위원회의 승인하에 진행되었다(승인 번호: KC20RISI0440).
대상 환자들은 수술 전 검사로 세극등현미경(BQ900®, Haag Streit AG, Köniz, Switzerland)을 이용한 전안부 및 안저검사, 빛간섭단층촬영(Spectralis®, Heidelberg Engineering, Heidelberg, Germany)을 시행하였다. 최대교정시력은 스넬렌시력표를 이용하여 측정한 후 통계 분석을 위해 logarithm of the minimum angle of resolution (logMAR)로 변환하였다. 수술 전날 자동비접촉안압계를 이용한 안압검사, 안구생체계측(IOL Master® 500, Carl Zeiss Meditec AG, Jena, Germany), 자동각막굴절력계(KR-1®, Topcon, Tokyo, Japan)를 이용하여 현성 굴절력(manifest refraction) 및 각막곡률값을 측정하였으며, 모든 검사는 숙련된 단일 검사자(M.K.)에 의해 시행되었다.
모든 수술은 숙련된 단일 술자(Y.H.P.)에 의해 시행되었고, 백내장수술 후 유리체절제술을 순차적으로 시행하였다. 모든 환자는 각막절개를 통한 수정체초음파유화술 및 인공수정체 낭내 삽입술을 시행받았고, 수술에는 동일한 인공수정체(Superflex® intraocular lens, Rayner Surgical, Worthing, UK)를 사용하였다. 백내장수술에 이어 표준 3포트 유리체절제술을 시행하였고, 유리체절제침은 망막박리 환자 3건에서만 23게이지를 사용하였고 나머지는 25게이지를 사용하였다. 모든 수술에서 가스 주입을 시행하였고, 술자의 판단에 따라 육플루오로화황(SF6)이나 과플루오로프로판(C3F8)을 사용하였다. 술자의 판단에 따라 공막절개창의 누출이 의심될 경우 8-0 흡수성봉합사를 이용한 공막절개창 봉합을 시행하였다.
대상자를 망막박리(group A), 망막앞막(group B)의 두 군으로 나누어 목표 굴절치, 수술 전, 수술 후 2, 6, 12개월째의 굴절력, 각막곡률값, 수술 전후 안압, 수술 전 전방깊이를 각각 비교하였다. 굴절력은 구면렌즈대응치(spherical equivalents = spherical power + one half cylinder power)로 환산하였으며 술 후 6개월째의 굴절력에서 SRK/T 공식을 사용하여 계산한 목표 굴절치의 차이를 예측오차로 계산하였다.
통계학적 분석은 IBM SPSS ver. 26.0 for Windows (IBM Corp., Armonk, NY, USA)을 사용하였다. 각 군에서 수술 전과 수술 후 6개월째의 굴절력과 각막곡률값의 비교는 Shapiro-Wilk, Kolmogorov-Smirnov 방법으로 정규성 검정한 후, paired t-test, Wilcoxon signed rank test를 이용하였으며, 각 군에서 이환된 눈과 반대안과의 안압 비교는 student t-test로 하였다. 각 군에서 나이, 수술 전 안압, 수술 후 6개월째의 안압, 안축장, 수술 전 전방깊이를 예측오차값과 상관관계가 있는지 확인하기 위해 로지스틱 회귀분석으로 분석하였으며, 망막박리군에서는 수술 전후 안압 차이, 망막앞막 군에서는 수술 전후의 중심망막두께와 그 차이가 예측오차에 영향을 주는 변수일 수 있어 추가하여 분석하였다. 단변량 선형회귀분석을 통해 분석 후 p<0.05인 의미 있는 변수들을 다시 다변량 선형 회귀분석하여 예측오차에 가장 큰 영향을 미치는 변수를 알아내었다. 유의수준은 0.05 미만(p-value<0.05)이면 통계적으로 유의한 것으로 간주하였다.
결 과
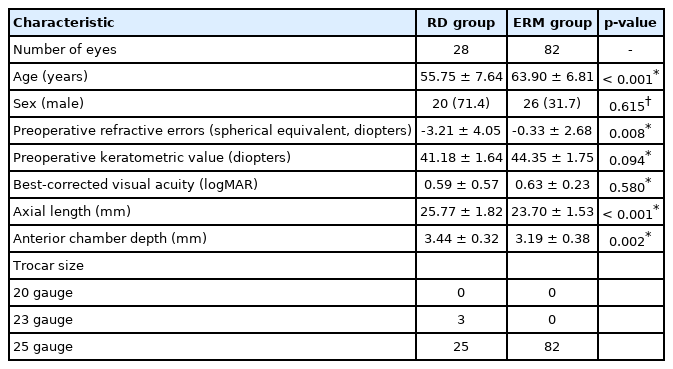
망막박리 28안, 망막앞막 82안을 대상으로 후향적 의무기록 분석을 시행하였다. 환자의 평균 연령은 망막박리군이 55.75 ± 7.64세, 망막앞막군이 63.90 ± 6.81세로 망막앞막군에서 유의하게 높았다(p<0.001). 수술 전 굴절력은 망막박리군에서 -3.21 ± 4.05 D, 망막앞막군에서 -0.33 ± 2.68 D (p=0.008)이며 각막곡률값은 각각 41.18 ± 1.64 D, 44.35 ± 1.75 D로 두 군 간 의미 있는 차이는 없었다(p=0.094). 최대교정시력은 망막박리군이 0.59 ± 0.57 logMAR, 망막앞막군은 0.63 ± 0.23 logMAR으로 두 군 간 차이는 없었으며 (p=0.580), 안축장은 25.77 ± 1.82 mm, 23.70 ± 1.53 mm로 망막박리군에서 유의하게 길었다(p<0.001). 수술 전 전방깊이도 망막박리군은 3.44 ± 0.32 mm, 망막앞막군은 3.19 ± 0.38 mm로 망막박리군이 유의하게 깊었다(p=0.002) (Table 1). 전체 110안 중 105안(95.45%)에서 공막절개창 봉합을 시행하였다.
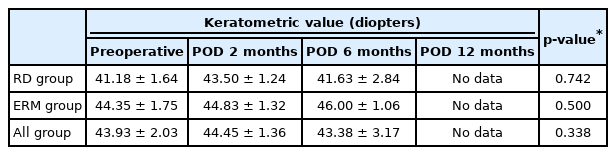
두 그룹 모두에서 수술 후 6개월째의 굴절력은 목표 굴절치에 비해 의미 있는 근시편위를 보였다. 전체 환자에서는 -0.85 ± 0.85 D, 망막박리군에서는 -0.92 ± 1.13 D, 망막앞막군에서는 -0.83 ± 0.78 D로 확인되었다(Table 2). 각막곡률값은 수술 후 6개월째 망막박리군에서 41.63 ± 2.84 D (p=0.742), 망막앞막군에서 44.83 ± 1.32 D (p=0.500)로 수술 전과 비교해 수술 후 의미 있는 차이는 보이지 않았다(Table 3).

Predicted and postoperative refractive outcome and prediction difference at 6 months after pars plana vitrectomy
수술 전 망막박리군에서는 수술안의 안압이 12.82 ± 3.36 mmHg로 반대안 15.32 ± 3.84 mmHg에 비해 안압이 의미있게 낮았으나(p=0.012), 망막앞막군에서는 수술안과 반대안의 안압에 유의한 차이가 없었다(p=0.880). 수술 후 6개월째 수술안과 반대안의 안압을 비교하였을 때, 망막박리군(p=0.705) 및 망막앞막군(p=0.378) 모두에서 수술안과 반대안의 안압에 유의한 차이가 없었다(Table 4).
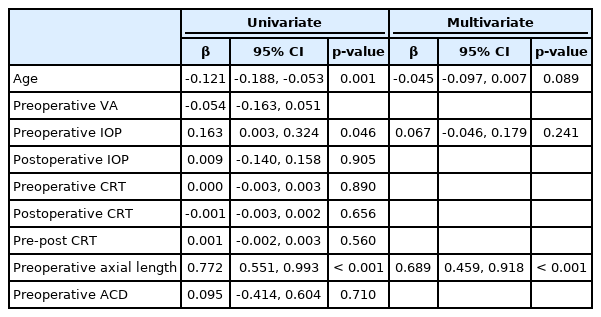
술 후 굴절력 예측오차와 각 인자들의 관계를 단변량 회귀분석한 결과, 망막박리군에서는 수술 후 6개월째 안압(β=-0.139, p=0.020) 및 안축장(β=0.235, p=0.018)이 예측오차와 통계적으로 유의한 연관성을 보였다. 다변량 회귀분석에서는 안축장만이 통계적으로 유의한 연관성을 보였다(β=0.189, p=0.036) (Table 5). 망막앞막군에서 시행한 단변량 회귀분석에서는 나이(β=-0.121, p=0.001), 수술 전 안압(β=0.163, p=0.046) 및 안축장(β=0.772, p<0.001)이 굴절력 예측오차와 통계적으로 유의한 연관성을 보였다. 다변량 회귀분석에서는 안축장만이 통계적으로 유의한 연관성을 보였다(β=0.689, p<0.001) (Table 6). 따라서 망막박리군 및 망막앞막군 모두에서 안축장이 유리체절제술과 백내장 병합수술 후 굴절력 예측오차를 예측하는 유의한 인자로 생각된다.
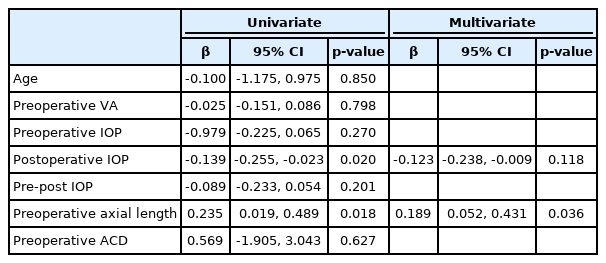
Univariate and multivariate regression analysis between refractive prediction error and variables (RD study population)
고 찰
본 연구는 망막박리와 망막앞막을 가진 환자들을 대상으로 하여 유리체절제술과 백내장수술을 동시에 시행하였을 때 목표 굴절력과 실제 굴절력의 오차를 비교하였다. 그 결과, 수술 후 6개월째 망막박리군에서 -0.92 D, 망막앞막군에서 -0.83 D의 근시편위를 보였다. 수술 후 굴절력 예측오차를 예측하는 인자로는 수술 전 안축장이 유의한 인자로 나타났으며, 나이, 안압, 수술 전 시력, 수술 전 전방깊이는 굴절력 예측오차와 유의한 상관관계를 보이지 않았다.
수술 후 굴절력에 영향을 미칠 수 있는 요인으로는 안축장의 변화, 각막난시의 변화, 가스 주입으로 인해 인공수정체가 앞으로 밀리는 경우 등이 있다. 그중 안축장 길이가 변하는 경우는 수술 전 낮았던 안압이 수술 후 증가하면서 공막 탄성에 의해 안축장이 길어져 발생할 수 있다. 특히 망막박리가 있는 눈은 안압이 낮아지는 것으로 알려져 있는데[12] 본 연구에서도 망막박리가 있는 눈은 수술 전 반대안과 비교하여 2.5 mmHg가량 안압이 낮았으며, 수술 후 평균 1.39 mmHg 상승하였다. 기존 연구에서[13] 망막박리안에서 평균 안압 1.7 mmHg 증가가 -0.43 D 근시편위를 유의하게 가져온다고 보고한 바 있는데, 본 연구에서도 술 전 안압은 유의하게 낮았지만 근시편위에 영향을 주는 변수를 분석하였을 때 안압과는 관계가 없는 것으로 확인되었다. 그 이유로 생각해 볼 수 있는 점은 기존 연구는 접촉식 초음파로 안축장을 측정하여 발생하는 함입 편향을 배제하지 못하였고, 본 연구에서는 비접촉식 생체계측기를 이용하여 함입 편향으로 인한 오차를 통제하였기 때문으로 생각된다.
공막절제침과 공막창 봉합 유무에 따라서 각막난시가 유발되어 술 후 굴절력에 영향을 줄 수 있다는 연구들도 있다. Zhang et al [15]은 무봉합 유리체절제술에서 초기 난시유발이 적다고 하였으며, 다른 연구들에서도 무봉합수술에 비해 봉합수술에서 술 후 1개월까지는 의미 있는 난시를 보였고 이후에는 차이가 없었다고 하였다[16,17]. 본 연구에서는 망막박리 3안을 제외하고 모두 25게이지 공막절제침을 사용하였으며, 대부분의 경우(95.45%) 공막창을 봉합하였다. 백내장과 유리체절제술의 병합수술을 대상으로 한 많은 연구들에서도 병합수술이 술 후 6개월째 각막곡률값에 영향을 주지 않는다는 것이 확인되었으며[8,13], 본 연구에서도 술 후 2, 6, 12개월째 결과값을 측정하였고 모든 시기에서 수술 및 공막창봉합이 난시나 굴절력에 의미 있는 영향을 주지 않은 것으로 확인되었다.
Danjo et al [18]는 유리체절제술 후 전방깊이의 변화가 생기고 유리체가 방수와 비교해 더 작은 굴절상수를 갖기 때문에 유리체절제술 자체로도 근시이행을 할 수 있다고 보고한 바 있다. 이와 반대로 인공수정체를 가지고 있는 환자에서 유리체절제술 후 가스를 주입하였을 때 전방깊이를 측정하였더니 줄어들지 않았다고 보고한 논문도 있었지만[10], 이 연구는 이미 백내장수술을 하여 인공수정체 위치가 고정되었을 것이며 증례 수가 적다는 한계가 있다. 최근 한 연구에서는 가스 주입 시 인공수정체의 위치와 전방깊이에 대하여 확인하기 위하여 백내장군, 가스 주입을 시행한 유리체절제술 병합수술군, 가스 주입을 하지 않은 유리체절제술 병합수술군을 비교하였다. 모든 군에서 수술 전에 비하여 전방깊이는 깊어졌지만, 백내장군과 가스 주입을 하지 않은 유리체절제술 병합수술군에 비하여 가스 주입을 한 군에서 인공수정체가 앞으로 밀려 전방깊이가 더 얕았고, 심지어 가스가 없어진 한 달 후에도 인공수정체는 뒤쪽으로 이동하지 않았고 전방깊이는 비슷하였다[19]. 본 연구도 망막앞막군과 망막박리군에서 모두 가스 주입을 하였기 때문에 수술 후 근시편위가 전방깊이의 변화에 영향을 받았을 가능성이 있으나, 수술 후 전방깊이에 대해 분석하지 못한 것은 본 연구의 한계점이다. 또한 백내장만 시행한 군과 예측 오차를 비교한다면 조금 더 명확한 결과를 얻을 수 있을 것으로 생각되어 추가적인 연구도 필요하겠다.
그 외에 유리체절제술 후 근시편위에 영향을 주는 인자들을 분석하였을 때 한 연구에서는 안축장이 길수록, 수술 전 시력이 좋지 않을수록 더 근시편위가 일어나는 경향이 있다고 하였다[8]. 또 다른 연구에서도 안축장이 길수록, 수술 전 근시의 정도가 심할수록, 술 전 망막두께가 두꺼울수록 근시편위가 심한 것으로 확인되었다[20]. 본 연구에서는 단변량 회귀분석 결과 망막박리군에서는 수술 후 안압과 안축장이, 망막앞막군에서는 나이, 수술 전 안압, 안축장이 유의한 변수로 확인되었다. 이 변수들로 다변량 회귀분석을 시행하였을 때 두 군 모두 안축장만이 유의하게 상관관계가 있는 것으로 나타나 기존 연구에 부합하는 결과를 보였다.
오랜 기간 동안 많은 연구에서 백내장과 유리체절제술의 동시 수술이 근시편위를 보이거나[6,7] 보이지 않는다[8,21,22]는 논란이 있었으며, 그 후에는 가스 주입 시에만 근시편위를 보인다는 연구[7,14,23]도 있었다. 하지만 이들은 망막질환의 특성에 따라 결과가 달라질 수 있음에도 질환을 구분하지 않고 연구 대상으로 포함하였거나, 여러 술자에 의해 다른 방법으로 수술하였거나, 오차가 생길 수 있는 측정기구를 이용하는 등의 한계가 있었기 때문에 본 연구에서는 이러한 변수들을 모두 제외하여 근시편위의 정도와 그 영향을 미치는 변수를 분석하였다는 데에 의의가 있다고 생각한다.
결론적으로 망막박리와 망막앞막을 대상으로 가스 주입을 포함한 유리체절제술과 백내장 병합수술을 시행하였을 때 두 군 모두 유의미한 근시편위를 보였으며, 수술 전 안축장 길이가 굴절력 예측오차를 예측하는 유의한 인자로 확인되었다. 따라서 이러한 근시편위 정도를 고려하여 인공수정체 도수를 결정해야 하며, 향후 수술 전후 전방깊이 분석에 따른 근시편위의 정밀한 원인 분석 및 각기 다른 망막질환에서의 굴절력 예측오차에 관한 추가적인 연구가 필요할 것으로 생각된다.
Notes
The authors have no conflicts to disclose.